
向15mL 0.1mol/L Ba(OH)2溶液中,滴加等浓度NH4Al(SO4)2溶液x mL,下列叙述错误的是
A.x=5时,溶液中有Ba2+、OH-、AlO2-,且OH-> AlO2-
B.x=7.5时,溶液中有NH4+、AlO2-,且NH4+=AlO2-
C.x=10时,溶液中有SO42-、NH4+,且H+> OH-
D.x=15时,溶液中有SO42-、NH4+、Al3+,且NH4+> Al3+
B
【解析】
试题分析:15mL 0.1mol/L Ba(OH)2溶液中氢氧化钡的物质的量为0.0015mol,n(Ba2+)=0.0015mol,n(OH-)=0.003mol;A、当x=5时,NH4Al(SO4)2的物质的量为0.0005mol,n(SO42-)=0.001mol,n(Al3+)=0.0005mol,n(NH4+)=0.0005mol。SO42-与Ba2+反应,SO42-不足,Ba2+剩余0.0005mol;0.0005molAl3+反应生成Al(OH)3消耗OH-的量为0.0015mol,溶液中没有Al3+,生成0.0005mol Al(OH)3,还剩余0.0015molOH-;然后与0.0005molNH4+反应消耗OH-的量为0.0005mol,溶液中NH4+完全反应,剩余0.001molOH-;0.0005mol Al(OH)3又完全溶解,生成0.0005molAlO2-,消耗0.0005molOH-,最终剩余0.0005molOH-.溶液中AlO2-水解,故OH->AlO2-,综上所述,溶液中有Ba2+、OH-、AlO2-,且OH->AlO2-,故A正确;B、当x=7.5时,NH4Al(SO4)2的物质的量为0.00075mol,n(SO42-)=0.0015mol,n(Al3+)=0.00075mol,n(NH4+)=0.00075mol.SO42-与Ba2+恰好反应,Ba2+没有剩余;0.00075molAl3+反应生成Al(OH)3消耗OH-的量为0.00225mol,溶液中没有Al3+,生成0.0005mo Al(OH)3,还剩余0.00075molOH-;然后与0.00075molNH4+恰好反应,溶液为氨水,故B错误;C、当x=10时,NH4Al(SO4)2的物质的量为0.001mol,n(SO42-)=0.002mol,n(Al3+)=0.001mol,n(NH4+)=0.001mol。SO42-与Ba2+反应,Ba2+不足,SO42-剩余0.0005mol;0.001molAl3+反应生成Al(OH)3消耗OH-的量为0.003mol,溶液中没有Al3+,生成0.001mol Al(OH)3,OH-完全反应,溶液中NH4+不反应,此时溶液为硫酸铵溶液,铵根离子水解,溶液呈酸性,综上所述,溶液中有SO42-、NH4+,且H+>OH-,故C正确;D、当x=15时,NH4Al(SO4)2的物质的量为0.0015mol,n(SO42-)=0.003mol,n(Al3+)=0.0015mol,n(NH4+)=0.0015mol.SO42-与Ba2+反应,Ba2+不足,SO42-剩余0.0015mol;0.0015molAl3+反应生成Al(OH)3消耗OH-的量为0.0045mol,OH-不足,溶液中0.001molAl3+反应,生成0.001mol Al(OH)3,溶液中剩余0.0005molAl3+,溶液中NH4+不反应,此时溶液为硫酸铵、硫酸铝溶液,铵根离子、铝离子水解,溶液呈酸性,综上所述,溶液中有SO42-、NH4+、Al3+,且NH4+>Al3+,故D正确,答案选B。
考点:考查离子方程式判断以及有关计算


科目:高中化学 来源:2011-2012学年山东省高三上学期期末检测化学试卷 题型:选择题
向15mL 0.1mol·L-1KOH溶液中逐滴加入0.2 mol·L-1甲酸(HCOOH,一元弱酸)溶液,溶液pH和加入的甲酸的体积关系曲线如右图所示,有关粒子浓度大小关系正确
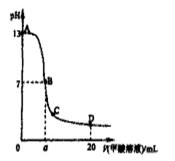
A.在A、B间任意一点c(K+) > c(HCOO-) > c(OH-) > c(H+)
B.在B点:c(K+) = c(HCOO-) > c(OH-) = c(H+),且a=7.5
C.在C点:c(HCOO-) > c(K+) > c(OH-) > c(H+)
D.在D点:c(HCOO-) + c(HCOOH) > 2c(K+)
查看答案和解析>>
科目:高中化学 来源: 题型:
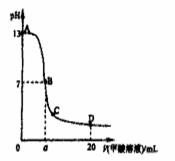
向15mL 0.1mol·L-1KOH溶液中逐滴加入0.2 mol·L-1甲酸(HCOOH,一元弱酸)溶液,溶液pH和加入的甲酸的体积关系曲线如右图所示,有关粒子浓度大小关系正确的是:
A.在A、B间任意一点c(K+) > c(HCOO-) > c(OH-) > c(H+)
B.在B点:c(K+) = c(HCOO-) > c(OH-) = c(H+),且a=7.5
C.在C点:c(HCOO-) > c(K+) > c(OH-) > c(H+)
D.在D点:c(HCOO-) + c(HCOOH) > 2c(K+)
查看答案和解析>>
科目:高中化学 来源: 题型:
向15mL 0.1mol·L-1KOH溶液中逐滴加入0.2mol·L-1甲酸(HCOOH,一元弱酸)溶液,溶液pH和加入的甲酸的体积关系曲线如右图所示,有关粒子浓度大小关系正确
A.在A、B间任意一点c(K+) > c(HCOO-)> c(OH-) > c(H+)
B.在B点:c(K+) = c(HCOO-) > c(OH-) = c(H+),且a=7.5
C.在C点:c(HCOO-) > c(K+) > c(OH-) >c(H+)
D.在D点:c(HCOO-) + c(HCOOH) > 2c(K+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com