



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ѧ��ѧ����Ҫ����������ʶ��Ȼ������ڵĸ��ָ����ġ�����Ļ�ѧ��Ӧ��̽�����Ļ�ѧ��Ӧ�ı��ʺ��ɣ�ͨ����ѧ��Ӧԭ��ģ���ѧϰ�����ǿ��ԱȽ���̵����⻯ѧ��ѧ�ľ��裬���ѧѧ���������������ѧ��ѧ��Ӧԭ��������������⣮
��ѧ��ѧ����Ҫ����������ʶ��Ȼ������ڵĸ��ָ����ġ�����Ļ�ѧ��Ӧ��̽�����Ļ�ѧ��Ӧ�ı��ʺ��ɣ�ͨ����ѧ��Ӧԭ��ģ���ѧϰ�����ǿ��ԱȽ���̵����⻯ѧ��ѧ�ľ��裬���ѧѧ���������������ѧ��ѧ��Ӧԭ��������������⣮| 1 |
| 2 |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ������ѧ��ѧ��Ӧԭ��������������⣺
������ѧ��ѧ��Ӧԭ��������������⣺| 1 |
| 2 |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
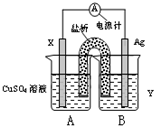
 ��2011?������һģ������������ԭ��Ӧ��2Ag+��aq��+Zn��s��=2Ag��s��+Zn2+��aq����Ƶ�ԭ�����ͼ��ʾ������������ȷ���ǣ�������
��2011?������һģ������������ԭ��Ӧ��2Ag+��aq��+Zn��s��=2Ag��s��+Zn2+��aq����Ƶ�ԭ�����ͼ��ʾ������������ȷ���ǣ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
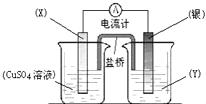 ����������ԭ��Ӧ��2Ag+��aq��+Cu��s��?Cu2+��aq��+2Ag��s����Ƶ�ԭ�����ͼ��ʾ������˵������ȷ���ǣ�������
����������ԭ��Ӧ��2Ag+��aq��+Cu��s��?Cu2+��aq��+2Ag��s����Ƶ�ԭ�����ͼ��ʾ������˵������ȷ���ǣ�������| A���缫X�IJ�����ͭ | B���������ҺY����������Һ | C�����缫Ϊ��ص������������ĵ缫��ӦΪ��Ag++e-?Ag | D�������е�������������ͭ��Һ���˶� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com