
人们对原子结构的认识有一个不断深入的过程,下列先后顺序中符合史实的是( )
①道尔顿提出的原子论 ②卢瑟福的原子结构行星模型
③波尔提出的原子力学模型 ④汤姆生提出的葡萄干面包原子模型
| A.①②④③ | B.①④②③ | C.②①④③ | D.①③②④ |
科目:高中化学 来源: 题型:单选题
短周期元素X、Y、Z、W在元素周期表中的相对位置如下图所示。下列说法正确的是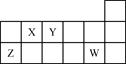
| A.原子半径的大小顺序:rZ>rY>rX |
| B.氢化物的稳定性强弱顺序:XH4>YH3>HW |
| C.Y的氢化物与W的氢化物化合所得产物中只含有共价键 |
| D.X、Y、Z、W四种元素的最高价氧化物对应水化物均能与强碱反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15;X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状态下的密度为0.76g ? L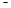 1;W的质子数是X、Y、Z、M四种元素质子数之和的1/2 。下列说法正确的是( )
1;W的质子数是X、Y、Z、M四种元素质子数之和的1/2 。下列说法正确的是( )
| A.原子半径:W>Z>Y>X>M |
| B.XZ2、X2M2、W2Z2均为共价化合物 |
| C.由X元素形成的单质不一定是原子晶体 |
| D.由Y、Z、M三种元素形成的化合物一定只有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
a、b、c、d、e是同周期的五种元素,a和b的最高价氧化物的水化物显碱性,且将a、b相连浸入稀硫酸中时,a溶解而b表面有气泡产生;c和d的气态氢化物的还原性d>c,五种元素的原子,得失电子后所形成的简单离子中,e的离子半径最小,则它们的原子序数由小到大的顺序是( )
| A.a、b、e、d、c | B.e、d、a、b、c |
| C.b、a、e、d、c | D.a、b、d、c、e |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法中正确的是
| A.电子云通常是用小黑点来表示电子的多少 |
| B.处于最低能量的原子叫基态原子 |
| C.能量高的电子在离核近的区域运动,能量低的电子在离核远的区域运动 |
| D.电子仅在激发态跃迁到基态时才会产生原子光谱 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
四种短周期元素在周期表中的相对位置如右表所示,下列说法错误的是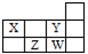
| A.X和Y元素的原子最外层电子数之和等于Z元素的原子最外层电子数的2倍 |
| B.Y元素的非金属性强于W元素的,其最高价氧化物水化物的酸性也强于W的 |
| C.X最简单氢化物溶于水呈碱性,Z最简单氢化物溶于水呈酸性 |
| D.W元素形成的单质可以从Z元素氢化物的水溶液中置换出Z单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断以下叙述正确的是
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.071 | 0.099 |
| 主要化合价 | +2 | +3 | +6、-2 | -1 | -1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列说法正确的是
| A.X2-的还原性一定大于Y- |
| B.由mXa+与nYb-得m+a=n-b |
| C.X、Y一定不是同周期元素 |
| D.若X的原子半径大于Y,则气态氢化物的稳定性一定是X大于Y |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素的四种离子aW3+、bX+、cY2-、dZ- 它们的电子层结构相同,下列关系正确的是
| A.质子数c>d | B.离子的还原性Y2->Z- |
| C.氢化物的稳定性H2Y>HZ | D.原子半径X<W |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com