
| n |
| V |
| n |
| V |


科目:高中化学 来源: 题型:
| A、CO2 |
| B、HCl(气态) |
| C、Fe(OH)3胶体 |
| D、NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
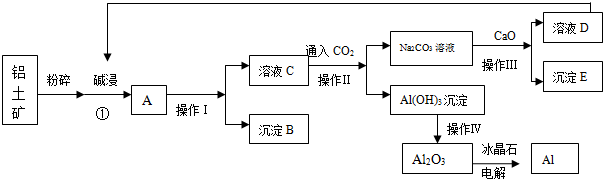
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 编号 | 0.01mol?L-1 酸性KMnO4溶液 | 0.1mol?L-1 H2C2O4溶液 | 水 | 1mol?L-1 MnSO4溶液 | 反应温度 /℃ | 反应时间 |
| Ⅰ | 2mL | 2mL | 0 | 0 | 20 | 125 |
| Ⅱ | 1mL | 0 | 20 | 320 | ||
| Ⅲ | 0 | 50 | 30 | |||
| Ⅳ | 2mL | 2mL | 0 | 2滴 | 20 | 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、-41.2kJ?mol-1 |
| B、+165.0kJ?mol-1 |
| C、-288.6kJ?mol-1 |
| D、+453.6kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 相关实验 | 预期目的 | |
| A. | 在少量食用碱中滴加食醋 | 探究食用碱是碳酸钠还是碳酸氢钠 |
| B. | 在食用盐中滴加少量淀粉液 | 探究食用盐是否为加碘盐 |
| C. | 用激光笔照射淀粉液 | 探究淀粉液是胶体还是溶液 |
| D | 将鸡蛋白溶于水后,滴加AgNO3溶液 | 验证蛋白质中含有氯元素 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com