
| A. | 都是白色的固体 | B. | 都能和水反应形成强碱溶液 | ||
| C. | 都是碱性氧化物 | D. | 焰色反应的颜色都是紫色 |
分析 A、Na2O是白色固体,Na2O2是淡黄色固体;
B、Na2O与水反应生成氢氧化钠,Na2O2与水反应生成氢氧化钠和氧气;
C、碱性氧化物是指能与酸反应生成盐和水的金属氧化物;
D、钠的焰色反应呈黄色.
解答 解:A、Na2O是白色固体,Na2O2是淡黄色固体,颜色不同,故A错误;
B、Na2O与Na2O2与水反应都能生成氢氧化钠,氢氧化钠是强碱,故B正确;
C、因Na2O2与酸反应生成盐、水和氧气,则Na2O2不属于碱性氧化物,故C错误;
D、Na2O和Na2O2中都含有钠元素,所以焰色反应的颜色都是黄色,故D错误.
故选B.
点评 本题考查钠的氧化物的性质,明确发生的化学反应及相关的概念是解答本题的关键,难度不大.


科目:高中化学 来源: 题型:实验题
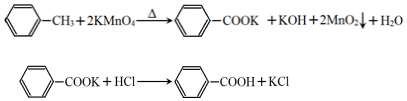
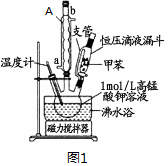
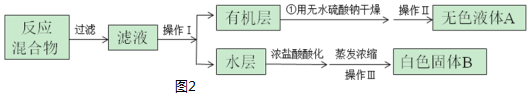
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
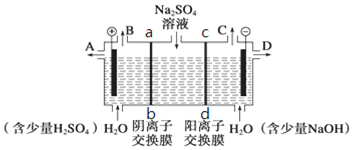
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙炔通入溴水中 | |
| B. | 乙烯通入酸性高锰酸钾溶液中 | |
| C. | 在镍作催化剂的条件下,苯与氢气反应 | |
| D. | 乙烷与氯气光照下发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 种 | B. | 2 种 | C. | 3 种 | D. | 4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=11的溶液 | B. | 4 g NaOH溶于水形成1L的水溶液 | ||
| C. | c(OH-)=0.12 mol•L-1 | D. | c(H+)=1×10-10 mol•L-1的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 物质(杂质) | 试剂 |
| A | Al2O3(SiO2) | 过量NaOH溶液 |
| B | CO2(HCl) | 饱和Na2CO3溶液 |
| C | Na2O2(Na2O) | O2/加热 |
| D | Al2O3(Fe2O3) | Al粉/加热 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com