
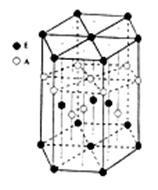
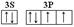 (1分)
(1分) 2CuCl2+2HCl(2分)
2CuCl2+2HCl(2分)

 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.主族元素的原子核外电子最后填入的能级是d能级或f能级 |
| B.镁型和铜型金属晶体的配位数均为12 |
| C.中心原子上的孤电子对不参与决定分子的空间结构 |
| D.分子中键角越大,价电子对相互排斥力越大,分子越稳定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱: H5IO6 HIO4.(填“>”、“<”或“=”)。H5IO6中α键与π键的个数比为 。
和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱: H5IO6 HIO4.(填“>”、“<”或“=”)。H5IO6中α键与π键的个数比为 。
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 离能(kJ·mol-1) | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.离子键 | B.共价键 | C.金属键 | D.配位键 E.氢键 F. 键 键 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com