
| A. | 1:3 | B. | 1:2 | C. | 2:3 | D. | 3:2 |
分析 根据n=cV计算出氢氧化钠的物质的量,根据反应方程式2NaOH+CO2═Na2CO3+H2O、NaOH+CO2=NaHCO3判断过量情况及反应产物,然后设出未知数计算出Na2CO3和NaHCO3的物质的量的比即可.
解答 解:1L 1.0mol/L 的NaOH溶液中含有氢氧化钠的物质的量为:1mol/L×1L=1mol,
根据2NaOH+CO2═Na2CO3+H2O可知,如果完全反应生成碳酸钠,需要消耗0.5mol二氧化碳,
若生成碳酸氢钠:NaOH+CO2=NaHCO3,则消耗1mol二氧化碳,
所以二者反应生成碳酸钠和碳酸氢钠的混合物,
设反应生成碳酸钠xmol、碳酸氢钠ymol,
则:2x+y=1mol、x+y=0.8mol,
解得:x=0.2mol、y=0.6mol,
则则所得溶液中Na2CO3和NaHCO3的物质的量的比为:0.2mol:0.6mol=1:3,
故选A.
点评 本题考查了化学方程式的计算,题目难度不大,注意根据反应物的物质的量先判断过量情况,从而得出反应产物,然后根据质量守恒定律列式计算,试题培养了学生的化学计算能力.


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:选择题
| A. | ④ | B. | ③ | C. | ①② | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将两种溶液都稀释100倍,醋酸的pH大于盐酸 | |
| B. | 用相同浓度的氢氧化钠溶液中和,消耗氢氧化钠的体积相等 | |
| C. | 分别加入质量相同的足量锌粉,开始时盐酸反应速率快 | |
| D. | 盐酸的浓度为0.01mol•L-1,醋酸浓度大于0.01mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚乙烯塑料的老化是由于发生了加成反应 | |
| B. | 加碘食盐中加入的I2有利于防止地方缺碘病 | |
| C. | 二氧化硫有漂白性,常用作棉、麻、纸张的漂白 | |
| D. | 汽车尾气污染物中含有氮的氧化物,是汽油不完全燃烧造成的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
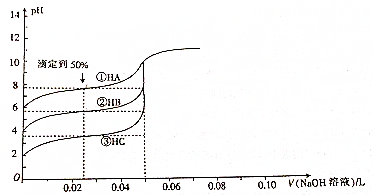
| A. | Ka(HA)>Ka(HB)>Ka(HC) | |
| B. | 滴定到50%时,溶液中:c(A-)>(B-)>(C-) | |
| C. | V(NaOH)溶液=50mL时,溶液中水的电离程度:①>②>③ | |
| D. | V(NaOH)溶液=50mL时,溶液pH的大小关系:pH(A)<pH(B)<pH(C) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
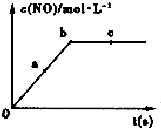 氮元素的单质及其化合物的研究和应用在工农业生产中有着非常重要的地位、工业制硝酸的主要反应之一是:
氮元素的单质及其化合物的研究和应用在工农业生产中有着非常重要的地位、工业制硝酸的主要反应之一是:| 深度/mol•L-1 时间/min | C(NH3) | c(O2) | c(NO) | c(H2O) |
| 起始 | 4.0 | 5.5 | 0 | 0 |
| 第2min | 3.2 | 4.5 | 0.8 | 1.2 |
| 第4min | 2.0 | 3.0 | 2.0 | 3.0 |
| 第6min | 2.0 | 3.0 | 2.0 | 3.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 元素 | Mn | Fe | |
| 电离能/mol | I1 | 717 | 758 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
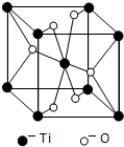
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 一定存在SO42-、CO32-、NH4+,可能存在K+、Cl-、Na+ | |
| B. | 一定存在SO42-、CO32-、NH4+、Cl-,一定不存在K+、Na+ | |
| C. | c(CO32-)=0.01 mol•L-1,c(NH4+)>c(SO42-) | |
| D. | 如果上述6种离子都存在,则c(Cl-)>c(SO42-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com