
科目:高中化学 来源: 题型:
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
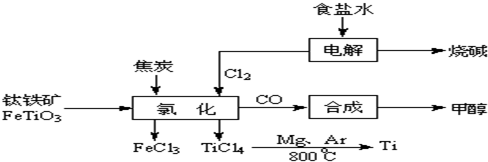
 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑ 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑ 2MgCl2(s)+Ti,在Ar气氛中进行的理由是:
2MgCl2(s)+Ti,在Ar气氛中进行的理由是:查看答案和解析>>
科目:高中化学 来源:2012-2013学年新疆乌鲁木齐一中高一(特长班)下期中考试化学卷(带解析) 题型:填空题
以甲醇、空气和氢氧化钾溶液为原料,金属铂为电极可构成普通的燃料电池。该电池的负极上的电极反应式为____________
查看答案和解析>>
科目:高中化学 来源:2015届新疆乌鲁木齐一中高一(特长班)下期中考试化学卷(解析版) 题型:填空题
以甲醇、空气和氢氧化钾溶液为原料,金属铂为电极可构成普通的燃料电池。该电池的负极上的电极反应式为____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com