
下列各组物质之间通过一步就能实现如图所示转化的是
选项 | 物质转化关系 | 甲 | 乙 | 丙 | 丁 |
A |
| Al2O3 | NaAlO2 | Al | Al(OH)3 |
B | Na2O | Na2O2 | Na | NaOH | |
C | CH2=CH2 | CH3CH2OH | CH3CHO | CH3COOH | |
D | NO | NO2 | N2 | HNO3 |
科目:高中化学 来源:2014-2015学年广东省六校联盟高三第三次联考理科综合化学试卷(解析版) 题型:选择题
下述根据下列操作和现象,所得结论正确的是
实验操作及现象 | 实验结论 | |
A | 分别向2 mL 0.1 mol·L-1 CH3COOH溶液和2 mL 0.1 mol·L-1 H3BO3溶液中滴加等浓度的NaHCO3溶液,前者有气泡产生,后者无明显现象 | 酸性:CH3COOH > H2CO3> H3BO3 |
B | 向浓度均为0.1 mol·L-1 NaCl 和NaI 混合溶液中滴加少量AgNO3溶液,产生黄色沉淀 | 溶度积:Ksp(AgCl)<Ksp(AgI) |
C | 向无水乙醇中加入浓H2SO4,加热,产生的气体通入酸性KMnO4溶液,紫色褪去 | 证明生成了乙烯 |
D | 将少量的溴水滴入NaI溶液中,再滴加CCl4,振荡、静置,溶液分为两层:上层溶液无色,下层溶液紫红色 | 氧化性:Br2>I2 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省上饶市高三上学期第一次联考化学试卷(解析版) 题型:选择题
下列有关离子方程式与所述事实相符且正确的是
A.用惰性电极电解CuCl2溶液2Cu2+2H2O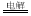 4H++O2↑+2Cu
4H++O2↑+2Cu
B.Ba(OH)2溶液中滴加NaHSO4溶液至中性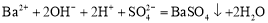
C.漂白粉溶液在空气中失效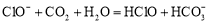
D.用氯化铁溶液和沸水反应制取氢氧化铁胶体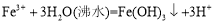
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省无锡市高三期末考试化学试卷(解析版) 题型:填空题
(14分)运用化学反应原理研究碳、氮的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
(1)某硝酸厂处理尾气中NO的方法是:催化剂存在时用H2将NO还原为N2。已知:
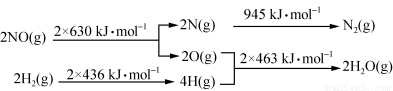
则氮气和水蒸气反应生成氢气和一氧化氮的热化学方程式是 。
(2)在压强为0.1 Mpa条件,将a mol CO和3a mol H2的混合气体在催化剂作用下转化为甲醇的反应如下:CO(g)+2H2(g) CH3OH(g) ΔH<0。
CH3OH(g) ΔH<0。
①该反应的平衡常数表达式为________________。
②若容器容积不变,下列措施可增大甲醇产率的是________。
A.升高温度
B.将CH3OH从体系中分离
C.充入He,使体系总压强增大
(3)某研究小组在实验室研究某催化剂效果时,测得NO转化为N2的转化率随温度变化情况如图。
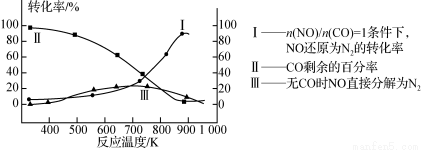
①若不使用CO,温度超过775 ℃,发现NO的分解率降低,其可能的原因为________;在n(NO)/n(CO)=1的条件下,应控制最佳温度在________左右。
②用CxHy(烃)催化还原NOx也可消除氮氧化物的污染。
写出C2H6与NO2发生反应的化学方程式________________。
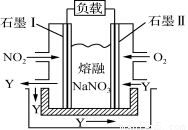
(4)以NO2、O2、熔融NaNO3组成的燃料电池装置如右图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,则该电极反应式为________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省无锡市高三期末考试化学试卷(解析版) 题型:选择题
下列实验操作的现象与结论正确的是
A.鉴别大豆油与矿物油的方法是分别加入足量氢氧化钠溶液共热,分层的是矿物油
B.某钠盐溶液中加入盐酸酸化的硝酸钡溶液,有白色沉淀产生,则该钠盐一定是硫酸钠
C.在KI淀粉溶液中滴入氯水变蓝,再通入SO2,蓝色褪去,表明SO2具有漂白性
D.向鸡蛋清溶液中,加入饱和(NH4)2SO4溶液,有白色沉淀产生,蛋白质发生了变性
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省无锡市高三期末考试化学试卷(解析版) 题型:选择题
常温下,在指定的溶液中一定能大量共存的离子组是
A.使pH试纸变蓝的溶液:Al3+、Na+、SO42 -、Cl-
B.c(SO32-)=0.1 mol·L-1的溶液:K+、MnO4- 、SO42 -、H+
C.c(H+)/c(OH-)=1×10-12的溶液:K+、AlO2- 、CO32 -、Na+
D.加入苯酚显紫色的溶液:Na+、NH4+ 、Cl-、I-
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省哈尔滨市高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列氯化物中,既能由金属和氯气直接参与化合制得,又能由金属和盐酸反应制得的是
A.CuCl2 B.FeCl2 C.MgCl2 D.FeCl3
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省哈尔滨市高二下学期第一次月考化学试卷(解析版) 题型:实验题
下图中的实验装置可用于制取乙炔。请填空:
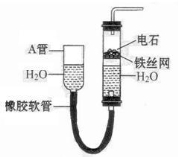
(1)图中,A管的作用是 。
制取乙炔的化学方程式是 。
(2)乙炔通入KMnO4酸性溶液中观察到的现象是 ,乙炔发生了 反应。
(3)乙炔通入溴的CCl4溶液中观察到的现象是 ,乙炔发生了 反应。
(4)为了安全,点燃乙炔前应 ,乙炔燃烧时的实验现象是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省宁波市高三十校联考理科综合化学试卷(解析版) 题型:选择题
废弃物资源化对于建设资源节约型社会具有重要的意义。铝灰是铝加工行业的废渣,其主要成分为Al、Al2O3,可能还含有KCl、FeO、Fe2O3、MgO、SiO2、MnO2中的若干种。为了确认其成分,某同学依次进行了以下实验:
①将过量的稀盐酸加入铝灰中,充分反应后过滤得到溶液甲和固体乙
②取少量溶液甲滴加AgNO3溶液,生成白色沉淀
③取少量溶液甲分成两等份,向其中一份滴加K3[Fe(CN)6]溶液,产生蓝色沉淀;向另一份滴加KSCN溶液,溶液变成血红色
④取少量溶液甲加入过量NaOH溶液,并置于空气中。充分反应后经过滤、洗涤、灼烧得到1.60g固体丙,将固体丙置于氢气流中加热充分反应后得到1.12g固体丁
根据以上实验现象或数据,该同学得出的结论正确的是:
A.根据①可推出铝灰中一定含有SiO2
B.根据②可推出铝灰中一定含有KCl
C.根据③可推出铝灰中一定含有FeO和Fe2O3
D.根据④可推出固体丙中一定不含MgO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com