
【题目】室温下,浓度均为0.1mol·L-1、体积均为Vo的HA、HB溶液,分别加水稀释至V,pH随![]() 的变化如图所示,下列说法正确的是
的变化如图所示,下列说法正确的是
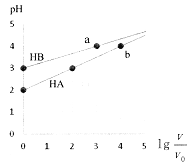
A. HA为强酸,HB为弱酸 B. 水的电离程度a点大于b点
C. 当pH=2时,HA溶液中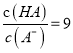 D. 等浓度等体积的HB与Na0H溶液充分反应后,离子浓度关系大小为:c(B-)> c(Na+)>c(H+)>c(OH-)
D. 等浓度等体积的HB与Na0H溶液充分反应后,离子浓度关系大小为:c(B-)> c(Na+)>c(H+)>c(OH-)
【答案】C
【解析】A.由图示可知,室温下浓度相等的HA和HB,HA的溶液pH小,即HA的酯性比HB强,但0.1mol/LHA的pH=2,说明HA也为弱酸,故A错误;B.HA和HB的水溶液中水的电离均受到抑制,a点和b点溶液的pH相等,说明水的电离程度相同,故B错误;C.0.1mol/LHA溶液中pH=2,则此时c(H+)=c(A-)=0.01mol/L,c(HA)=0.1mol/L-0.01mol/L=0.09mol/L, 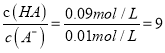 ,故C正确; D.等浓度等体积的HB与Na0H溶液充分反应后得到NaB溶液,因B-的水解溶液显碱性,离子浓度关系大小为: c(Na+)>c(B-)>c(OH-)>c(H+),故D错误;答案为C。
,故C正确; D.等浓度等体积的HB与Na0H溶液充分反应后得到NaB溶液,因B-的水解溶液显碱性,离子浓度关系大小为: c(Na+)>c(B-)>c(OH-)>c(H+),故D错误;答案为C。


科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度溶液的正确步骤的顺序是:
①把已冷却的溶液用玻璃棒小心引流到容量瓶中;②把称量好的溶质放在烧杯里用水溶解;③轻轻振荡容量瓶,使溶液混合均匀;④洗涤烧杯内壁,把洗涤液全部注入容量瓶;⑤定容;⑥盖紧容量瓶,反复上下颠倒摇匀。
A. ①②③④⑤⑥ B. ②③①④⑤⑥ C. ②①④⑤③⑥ D. ②①④③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学气敏传感器可用于检测环境中NH3的含量,其工作原理示意图如下。

下列说法不正确的是
A. O2在电极b上发生还原反应
B. 溶液中OH+向电极a移动
C. 负极的电极反应式为:2NH3-6e-+6OH-=N2+6H2O
D. 反应消耗的NH3与O2的物质的量之比为4:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产和生活密切相关,下列说法正确的是
A. 乙烯是化学物质,不可用作水果的催熟剂
B. 煤经过气化和液化等物理变化可转化为清洁燃料
C. 石油是混合物,经分馏后得到汽油、煤油和柴油等纯净物
D. 汽油与水互不相溶,但不可以用裂化汽油萃取溴水中的溴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取的乙炔气体中常混有少量H2S、CO2和水蒸气,为了得到干燥纯净的乙炔气体,选择最简便的实验方案有( )
A.通过NaOH后,通过浓H2SO4,再通过石灰水
B.通过CuSO4溶液后再通过石灰水
C.通过五氧化磷,再通过无水CaCl2
D.通过足量的碱石灰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若以w1和w2分别表示物质的量浓度为c1 mol/L和c2 mol/L H2SO4溶液的质量分数,且2w1=w2,则下列推断正确的是
A. 2c1=c2 B. 2c2=c1 C. c1<c2<2c1 D. c2>2c1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸钠、碳酸氢钠是日常生产生活中常用的两种盐。在实验室中制取NaHCO3的方法有多种。请
依据下列方法回答问题:
方法一:模拟工业“侯氏制碱法”制取:(原理NaCl+H2O+CO2+NH3 = NaHCO3↓+NH4Cl)
第一步:连接好装置,检验气密性,在仪器内装人药品。
第二步:让某一装置先发生反应,直到产生的气体不能再在Ⅲ中溶解,再通入另一装置中产生的气体,片刻后,Ⅲ中出现固体。继续向Ⅲ中通入两种气体,直到不再有固体产生。
第三步:分离Ⅲ中所得的混合物,得到NaHCO3固体。
第四步:向滤液中加入适量的某固体粉末,有NH4Cl晶体析出。
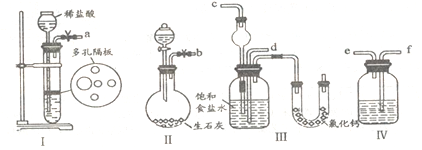
(1)图中所示装置的连接顺序是:a接f;e接________;b接_________(填接口编号)。
(2)I中盛放稀盐酸的仪器名称是_____________,IV中应选用的液体为________________。
(3)第二步中让_____________ (填序号)装置先发生反应。
(4)第四步中所加固体粉末为________。所得的晶体中常含有少置的NaCl和NaHCO3(约占5%~8%),请设计一个简单的实验,不使用其他任何试剂,证明所得晶体大部分是NH4Cl。简要写出操作和现象______________________。
方法二:把CO2通人饱和Na2CO3溶液制取NaHCO3。装置如下图所示(气密性已检验,部分夹持装置略):

(5)请结合化学平衡移动原理解释B中溶液的作用_________________。
(6)当C中有大量白色固体析出时,停止实验,将固体过滤、洗涤、干燥备用。为确定固体的成分,实验小组设计方案如下(取一定量的固体,配成溶液作为样液,其余固体备用):
①方案1:取样液与澄清的Ca(OH)2溶液混合,出现白色沉淀。
实验小组对现象产生的原理进行分析,认为该方案不合理,理由是________________。
②方案2:取样液与BaCl2溶液混合,出现白色沉淀并有气体产生。
实验小组认为固体中存在NaHCO3,其离子方程式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色透明的酸性溶液中,能大量共存的离子组是( )
A. Na+ 、K+、SO42-、HCO3 B. Cu2+、K+、SO42-、NO3
C. Na+、 K+、Cl、 NO3 D. Fe3+、K+、SO42-、Cl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com