
���� ��1�������£�Fe��Al��Ũ���ᷢ���ۻ�����Ũ���������ˮ�ԡ���ˮ�Ժ�ǿ�����ԣ�Ũ����ȶ��������ֽ⣻
��2���Ʊ�����ͭʱ����������Ի�������Ⱦ�ĸ���Ʒ��������ɫ��ѧ��
��3��ϡ�����ͭ��Ӧ��������ͭ��NO��ˮ��
��4�����������£�˫��ˮ��Cu�������ӷ���������ԭ��Ӧ����ͭ���ӡ�ˮ��
��� �⣺��1�������£�Fe��Al��Ũ���ᷢ��������ԭ��Ӧ������һ�����ܵ������ﱡĤ����ֹ��һ�����������������Ϊ�ۻ�����Ũ���������ˮ�ԡ���ˮ�Ժ�ǿ�����ԣ��ܽ�ֽ���е�H��OԪ����2��1ˮ����ʽ��ȥ��������ˮ�ԣ�����ֽ�ű��ɫ��Ũ����ȶ��������ֽ⣬��������Ӧ�ñ�������ɫ�Լ�ƿ�У�
�ʴ�Ϊ��ǿ��������ˮ�����ȶ���
��2���ٲ����ж���������������ڲ����ж�NO���۲������Ի�������Ⱦ�ĸ���Ʒ�����Է��ϡ���ɫ��ѧ��˼����Ǣۣ��ʴ�Ϊ���ۣ�
��3��ϡ�����ͭ��Ӧ��������ͭ��NO��ˮ����Ӧ�����ӷ���ʽΪ3Cu+8H++2NO3-=2NO��+3Cu2++2H2O���ʴ�Ϊ��3Cu+8H++2NO3-=2NO��+3Cu2++2H2O��
��4�����������£�˫��ˮ��Cu�������ӷ���������ԭ��Ӧ����ͭ���ӡ�ˮ����Ӧ�Ļ�ѧ����ʽCu+H2O2+2HCl=CuCl2+2H2O���ʴ�Ϊ��Cu+H2O2+2HCl=CuCl2+2H2O��
���� ���⿼��Ũ���ᡢ��������ʣ�Ϊ��Ƶ���㣬Ũ�����Ũ���ᶼ����ǿ�����ԣ���Ũ���ỹ������ˮ�Ժ���ˮ�ԣ�Ũ������в��ȶ��ԣ�ע�����֪ʶ���ܽ���ɣ�


 ��˼ά������ҵϵ�д�
��˼ά������ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaOH��Һ | B�� | Na2CO3��Һ | C�� | ���� | D�� | Na2SiO3��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | PHֵ��Ϊ12�İ�ˮ������������Һ��10 mL���ֱ��ˮϡ����100 mL����ˮ��Һ��PHֵ�仯�ϴ� | |
| B�� | ��ͭƬ����Ũ�����У�������ʵ������˵��ͭ�����Ũ�����з����ۻ� | |
| C�� | FeI2����Һ�У�����ͨ�������������ٵμ�����CCl4�������ã��²�Һ��Ϊ��ɫ | |
| D�� | ��Ͳ���ζ��ܡ�����ƿ������������ȡҺ�壬��Ͳ���ζ��ܶ��С�0���̶ȣ���Ͳ��0���̶������棬�ζ��ܡ�0���̶������棬����ƿ�б����������̶ȣ��ζ��ܺ�����ƿʹ��ǰ����Ҫ����Ƿ�©ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
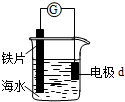
| A�� | dΪʯī��������d���뵼�߽�����Ƭ | |
| B�� | dΪͭƬ��ͭƬ�ϵ缫��ӦΪ��O2+2H2O+4e-�T4OH- | |
| C�� | dΪп�飬��Ƭ���ױ���ʴ | |
| D�� | dΪþƬ����Ƭ�ϵ缫��ӦΪ��2H++2e-�TH2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡ���� | B�� | ��ˮ | C�� | AgNO3 ��Һ | D�� | NaOH��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��H+��aq��+OH- ��aq���TH2O��l������H=-57.3 kJ•mol-1����֪��1 mol������������Һ�뺬0.5 mol�����ϡ��Һ��ϣ��ų���������57.3 kJ | |
| B�� | ��H2O��g���TH2O��l����H=-44.0kJ•mol-1��֪�Ƿ��ȷ�Ӧ | |
| C�� | ��SO2��g��+0.5O2��g���TSO3��g����H=-98.3 kJ•mol-1��֪�����ܱ������г���2 mol SO2��1 mol O2��ַ�Ӧ�ų�����Ϊ196.6 kJ | |
| D�� | �ɡ�G=��H-T��S��֪�����з��ȷ�Ӧ�����Է����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
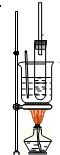 ʵ������ȡ�������ķ�����ͼ��ʾ��
ʵ������ȡ�������ķ�����ͼ��ʾ�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��� | B�� | �ڶ� | C�� | �ٶ� | D�� | ���ж� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com