
| A�� | ��t��ʱ��0.05mol•L-1��Ba��OH��2��ҺpH=11��t=25�� | |
| B�� | �����£���pH=a�Ĵ�����Һ�м���������Ũ�ȵ������pH=a+1 | |
| C�� | �����£���c1mol•L-1�İ�ˮ��c2mol•L-1�������������pH=7����c1��c2 | |
| D�� | �������pH��CH3COOH��Һ������ֱ����������۷�Ӧ����������H2�������� |
���� A.0.05mol•L-1��Ba��OH��2��ҺpH=11����Kw=10-12�����¶ȴ���25�棻
B����pH=a�Ĵ�����Һ�м���������Ũ�ȵ��������Һ������ǿ��
C�������£���c1mol•L-1�İ�ˮ��c2mol•L-1�������������pH=7�����Ϻ�ΪNH4Cl��NH3��H2O�����Һ���������ʵ�������HCl���ʵ�����
D��pH��ȵ�CH3COOH��Һ��������������Ũ����ȣ�����Ϊ������ʣ���ͬ�����´������ʵ���Զ����HCl���ʵ�����
��� �⣺A.0.05mol•L-1��Ba��OH��2��Һ��c��OH-��=0.1mol/L����ҺpH=11����Kw=10-12�����¶ȴ���25�棬��A����
B����pH=a�Ĵ�����Һ�м���������Ũ�ȵ��������Һ������ǿ��pH��С����B����
C�������£���c1mol•L-1�İ�ˮ��c2mol•L-1�������������pH=7�����Ϻ�ΪNH4Cl��NH3��H2O�����Һ���������ʵ�������HCl���ʵ�������c1��c2����C��ȷ��
D��pH��ȵ�CH3COOH��Һ��������������Ũ����ȣ�����Ϊ������ʣ���ͬ�����´������ʵ���Զ����HCl���ʵ�����Al����������ȫ��Ӧ�������������������࣬��D����
��ѡ��C��
���� ���⿼��������ʵ��롢��ҺpH�йؼ��㡢ˮ�����ӻ�������ˮ��ȣ�ע��ˮ�����ӻ����¶�Ӱ�죮


 Ӣ��СӢ������Ĭдϵ�д�
Ӣ��СӢ������Ĭдϵ�д� �����ҵ���������ͯ������ϵ�д�
�����ҵ���������ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
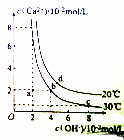
| A�� | 20��ʱ��Ca��OH��2�ܽ�ȴ���30��ʱ��Ca��OH��2���ܽ�� | |
| B�� | 30��ʱ��Ca��OH��2�ı�����Һ�м�������NaOH���壬Ca��OH��2��Ksp���� | |
| C�� | 30��ʱ��Ca��OH��2��Ksp����3.2��10-5 | |
| D�� | 20��ʱ����Ca��OH��2�ı�����Һ�м�������CaO���岢ά���¶Ȳ��䣬��Һ��pH���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ����������ϡ���ᷴӦ | B�� | ������ͭ��ϡ���ᷴӦ | ||
| C�� | ϡ������������ط�Ӧ | D�� | �������ƺ����ᷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Һ��pH���� | B�� | NH3•H2O�ĵ���ƽ�ⳣ������ | ||
| C�� | NH3•H2O�ĵ���̶����� | D�� | NH3•H2O��Һ����������Ũ�ȼ�С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
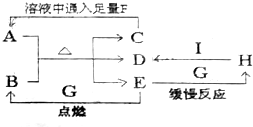 ��֪A������θ�����֢��һ��ҩ����B��һ�ֵ���ɫ���壬A��B�����ʵ���֮��1��1��ϼ��ȣ�������ת����ϵ��
��֪A������θ�����֢��һ��ҩ����B��һ�ֵ���ɫ���壬A��B�����ʵ���֮��1��1��ϼ��ȣ�������ת����ϵ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��

| A�� | ���ղ������������н��� | |
| B�� | ��XΪ�ռ��ZΪ����������aΪ����ɫ���������� | |
| C�� | ��XΪ���ᣬ��ZΪCO2����Һ��ֻ��NaCl��Na2CO3 | |
| D�� | ͼʾ�������ķ�Ӧ�����У��ֽⷴӦ�����ֽⷴӦ��������ԭ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����ϩ����Ҫ�Ļ����л�ԭ�ϣ���ҵ�����ұ���C6 H5-CH2 CH3��Ϊԭ�ϣ����ô�����ķ�����ȡ����ϩ��C6 H5-CH=CH2���ķ�Ӧ����ʽΪ��
����ϩ����Ҫ�Ļ����л�ԭ�ϣ���ҵ�����ұ���C6 H5-CH2 CH3��Ϊԭ�ϣ����ô�����ķ�����ȡ����ϩ��C6 H5-CH=CH2���ķ�Ӧ����ʽΪ��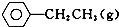 ?����
?���� �TCH2��g��+H2��g��
�TCH2��g��+H2��g��| ��ѧ�� | C-H | C-C | C=C | H-H |
| ����/kJ/mol | 412 | 348 | 612 | 436 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 100mL 1mol•L-1��NaCl��Һ | B�� | 150mL 1mol•L-1��MgCl2��Һ | ||
| C�� | 200mL 1mol•L-1��HCl��Һ | D�� | 10mL 1mol•L-1��AlCl3��Һ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com