
科目:高中化学 来源:2015-2016学年湖北省枣阳市高二下期中化学试卷(解析版) 题型:选择题
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速度,且不影响生成氢气的总量,可向盐酸中加入适量的
A.NaOH(固体) B.H2O
C.NH4Cl(固体) D.CH3COOH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省宜昌市高二下期中化学试卷(解析版) 题型:选择题
某烃含碳、氢原子物质的量之比为1:2,该烃对氮气的相对密度为2,该烃可使溴水褪色,该烃的二氯代物有四种同分异构体,该烃为
A.CH3CH2CH2CH3 B.CH2=CH—CH3
C.CH2=CH—CH2—CH3 D.CH2=C(CH3)2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省宜昌市高二下期中化学试卷(解析版) 题型:选择题
下列依据热化学方程式得出的结论正确的是
A.已知2H2(g)+O2(g)=2H2O(g);△H=-483.6 kJ·mol–1,则氢气的燃烧热为241.8kJ·mol–1
B.已知C(石墨,s)=C(金刚石,s);△H>0,则金刚石比石墨稳定
C.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=–57.4kJ·mol–1,则含20.0g溶质的NaOH稀溶液与稀醋酸完全中和,放出的热量小于28.7kJ
D.已知:2C(s)+2O2(g)=2CO2(g) △H1;2C(s)+O2(g)=2CO(g) △H2,则△H1>△H2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省襄阳市高一下期中化学试卷(解析版) 题型:填空题
CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值的化学品是目前的研究方向。
(1)已知:CH4(g) + 2O2(g)=CO2(g) + 2H2O(g) ΔH1 = a kJ•mol-1
CO(g) + H2O (g)=CO2(g) + H2 (g) ΔH2 = b kJ•mol-1
2CO(g) + O2(g)=2CO2(g) ΔH3 = c kJ•mol-1
反应CO2(g) + CH4(g) 2CO(g) + 2H2(g) 的ΔH= kJ•mol-1。
2CO(g) + 2H2(g) 的ΔH= kJ•mol-1。
(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。
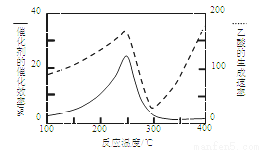
① 在不同温度下催化剂的催化效率与乙酸的生成速率如图8所示。250~300℃时,温度升高而乙酸的生成速率降低的原因是 。
② 为了提高该反应中CH4的转化率,可以采取的措施是 。
③ 将Cu2Al2O4溶解在稀硝酸中的离子方程式为 。
(3)以CO2为原料可以合成多种物质。
① 利用FeO吸收CO2的化学方程式为:6FeO + CO2=2Fe3O4 + C,则反应中每生成1molFe3O4,转移电子的物质的量为 mol。
② 以氢氧化钾水溶液作电解质进行电解,在铜电极上CO2可转化为CH4,另一电极石墨连接电源的 极,则该电解反应的化学方程式为
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省襄阳市高一下期中化学试卷(解析版) 题型:选择题
反应 A+B→C(△H<0)分两步进行 ①A+B→X (△H>0)②X→C(△H<0)下列示意图中,能正确表示总反应过程中能量变化的是( )
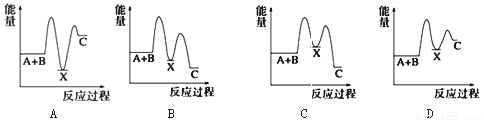
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省襄阳市高一下期中化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图。下列说法正确的是( )
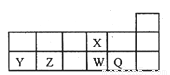
A.Y、Z的常见氧化物可通过加入过量的NaOH溶液来分离
B.其氢化物的稳定性由弱到强的顺序是Q、W、Z
C.元素Y、Z、W、Q的原子半径依次增大
D.Y单质做的容器可盛装W的最高价氧化物对应的水化物的浓溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二下期中化学试卷(解析版) 题型:填空题
硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3MgO、CaO等,生产工艺流程图如下:

(1)将菱锌矿研磨成粉的目的是_____。
(2)完成“氧化除铁”步骤中反应的离子方程式:□Fe(OH)2+□____+□_____=□Fe(OH)3+□CI-
(3)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O和H,摩尔质量为89g/mol,化学式是_______。以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时针铁矿转化为Fe(OH)2,该电池放电反应的化学方程式是__________。
(4)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为______。
沉淀化学式 | Mg(OH)2 | Zn(OH)2 | MgCO3 | CaCO3 |
开始沉淀的pH | 10.4 | 6.4 | — | — |
沉淀完全的pH | 12.4 | 8.0 | — | — |
开始溶解的pH | — | 10.5 | — | — |
Ksp | 5.6× | — | 6.8× | 2.8× |
(5)工业上从“滤液3”制取MgO过程中,合适的反应物是______(选填序号)。
a.大理石粉 b.石灰乳 c.纯碱溶液 d.氨水
(6)“滤液4”之后的操作依次为______、_______、过滤,洗涤,干燥。
(7)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于________(用代数式表示)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古杭锦后旗奋斗中学高一下期中化学卷(解析版) 题型:选择题
X、Y、Z均为短周期元素,在周期表中的位置如下图所示,下列叙述正确的是( )
Z | ||
Y | ||
X |
A.X一定是活泼金属
B.Y的最高价氧化物是酸性氧化物
C.Z的单质是双原子分子
D.氢化物的稳定性:Y>X
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com