
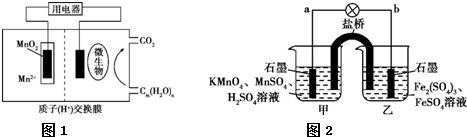
���� ��1��PbCl2ͨ����ѧ��Ӧ���������CO���壬��CO��PbCl2ӦΪ��Ӧ����÷�Ӧ�ķ�Ӧ������������CO��Pb��H2O��HCl��PbCl2��һ��δ֪����X������Ԫ���غ���жϳ�Pb��HClӦΪ�����������Ԫ���غ��֪H2OΪ��Ӧ�����Ԫ���غ����д���÷�Ӧ�ķ���ʽ�����ݷ���ʽ��֪X�Ļ�ѧʽ��
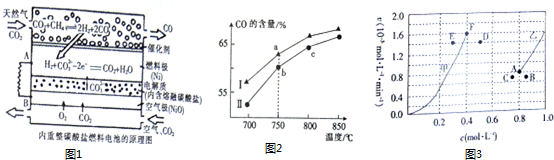
��2������ͼ��֪����ȼ�ϵ���У�ͨ������������̼��Ӧ����������һ����̼��1mol�����������2mol����������ʧȥ���ӷ���������Ӧ����õ缫Ϊԭ��صĸ����������缫��ӦʽΪ��H2-2e-+CO32-=CO2+H2O��ͨ�������CO2�Ļ������һ��Ϊԭ��ص�������������ԭ��Ӧ���缫��ӦʽΪO2+4e-+2CO2=2CO32-�����������������ӵ�ʧ�غ�ɼ���������������������
��3������CaCO3��KspΪ2.5��10-9���ɼ����̼��Ʊ�����Һ��̼��Ƶ�Ũ�ȣ����������̼��Ƶ��ܽ�ȣ�
��4���ٸ���ͼ3��֪�������¶����ߣ�CO�ĺ�������˵��ƽ�������ƶ������Ը÷�Ӧ������ӦΪ���ȷ�Ӧ�������¶ȶ�ƽ���ƶ���Ӱ��ɴ��⣻
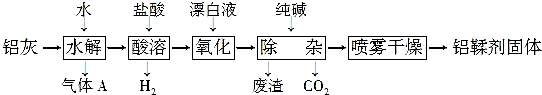
��CH4��CO2����ʼ�����ʵ���Ũ�Ⱦ�Ϊ1.0 mol•L-1�������ŷ�Ӧ�Ľ��У������Ũ�Ȼ�Խ��ԽС������Ӧ����Ҳ��Խ��ԽС���ݴ��жϣ�����ͼ��֪����Ӧƽ��ʱͼ�ж�Ӧ�ĵ�ӦΪA��F�㣬���º�Ӧ���ʼ�С��ƽ�������ƣ������Ũ�Ȼ����ݴ��жϣ�
��� �⣺��1��PbCl2ͨ����ѧ��Ӧ���������CO���壬��CO��PbCl2ӦΪ��Ӧ����÷�Ӧ�ķ�Ӧ������������CO��Pb��H2O��HCl��PbCl2��һ��δ֪����X������Ԫ���غ���жϳ�Pb��HClӦΪ�����������Ԫ���غ��֪H2OΪ��Ӧ��ø��ݻ��ϼ�������֪����Ӧ�ķ���ʽ��д��PbCl2+CO+H2O=Pb+2HCl+X������X�Ļ�ѧʽΪCO2��
�ʴ�Ϊ��CO2��
��2������ͼ��֪����ȼ�ϵ���У�ͨ������������̼��Ӧ����������һ����̼��1mol�����������2mol����������ʧȥ���ӷ���������Ӧ����õ缫Ϊԭ��صĸ����������缫��ӦʽΪ��H2-2e-+CO32-=CO2+H2O��ͨ�������CO2�Ļ������һ��Ϊԭ��ص�������������ԭ��Ӧ���缫��ӦʽΪO2+4e-+2CO2=2CO32-��������Ϊ3.36L����״������ͬ������0.15molʱ����������Ϊ0.3mol�������缫��Ӧʱת�Ƶ��ӵ����ʵ���Ϊ0.6mol�����ݷ�ӦO2+4e-+2CO2=2CO32-����ʱ���������ĵ�����Ϊ0.15mol��������̼Ϊ0.3mol����������������ʵ���Ϊ0.75mol�����Թ����Ŀ����Ͷ�����̼�����������ʵ���Ϊ1.05mol�������Ϊ23.52L��
�ʴ�Ϊ��������O2+4e-+2CO2=2CO32-��23.52��
��3������CaCO3��KspΪ2.5��10-9��֪��̼��Ʊ�����Һ��̼��Ƶ����ʵ���Ũ��Ϊ$\sqrt{2.5��10-9}$mol/L=5.0��10-5 mol/L������̼��Ƶ��ܽ��Ϊ$\frac{5.0��10{\;}^{-4}��100}{1000}��100g$=5.0��10-4 g��
�ʴ�Ϊ��5.0��10-4��
��4���ٸ���ͼ3��֪�������¶����ߣ�CO�ĺ�������˵��ƽ�������ƶ������Ը÷�Ӧ������ӦΪ���ȷ�Ӧ��ƽ�ⳣ��ֻ���¶�Ӱ�죬ab������¶���ͬ������Ka=Kb��c����¶ȸ���b�㣬�����¶�ƽ�������ƶ�������c���CO�ĺ�������b�㣬
�ʴ�Ϊ��=��c����¶ȸ���b�㣬�����¶�ƽ�������ƶ���
��CH4��CO2����ʼ�����ʵ���Ũ�Ⱦ�Ϊ1.0 mol•L-1�������ŷ�Ӧ�Ľ��У������Ũ�Ȼ�Խ��ԽС������Ӧ����Ҳ��Խ��ԽС����������v��-c��CH4�����Ӧ������ͼ3�����������ߣ�����ͼ��֪����Ӧƽ��ʱͼ�ж�Ӧ�ĵ�ӦΪA��F�㣬���º�Ӧ���ʼ�С��ƽ�������ƣ������Ũ�Ȼ��������Դ�ʱ����Ӧ��ƽ������ΪӦΪB�㣬CO��Ũ�Ȼ��С����Ӧ��ΪE��
�ʴ�Ϊ���ң�B��E��
���� ���⿼�黯ѧƽ��ͼ��Ӱ�컯ѧƽ������ء���ѧƽ�ⳣ�����������ܽ�ƽ����㡢�绯ѧ�ļ���ȣ�����ʱע���������ԭ�ĽǶ��ж�ԭ��ص��������Լ��缫����ʽ����д������ԭ���ǹؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| H������ | �ƶ�H����ɺͽṹ |
| H��ȫȼ�յIJ���ֻ��CO2��H2O | ��ɣ��϶���̼��������Ԫ�أ�Ҳ���ܺ���Ԫ�� |
| H���Ҵ���һ�������·�Ӧ�������ɾ��й���ζ�����ʣ��ҽṹ��ֻ�������ֹ����� | ��ɣ�����OԪ�� |
| 1.34gH�ֱ���������̼��������Һ���Ʒ�Ӧ�����ɱ�״���µ���������ֱ�Ϊ0.448L��0.336L | ��ɣ���������-COOH��һ��-OH |
| H��̼����֧�� | �ṹ��ʽ��HOOCCH��OH��CH2COOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C | B�� | CO | C�� | CH4 | D�� | CH3CH2OH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| Ԫ�ش��� | X | Y | Z | W |
| ԭ�Ӱ뾶/pm | 160 | 143 | 70 | 66 |
| ��Ҫ���ϼ� | +2 | +3 | +5��+3��-3 | -2 |
| A�� | X��YԪ�صĽ�����X��Y | |
| B�� | Y������������Ӧ��ˮ����������ϡ��ˮ | |
| C�� | һ�������£�W���ʿ��Խ�Z���ʴ����⻯�����û����� | |
| D�� | �����£�Z������W�ij�������ֱ������ZW2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | Ŀ�� | ʵ�� | ���� |
| A | ����CO2�����л���SO2 | ������ͨ��ʢ�������ij���ʯ��ˮ�е�ϴ��ƿ�� | ʯ��ˮ����� |
| B | �����ɫ����Fe3O4�к���+3����Ԫ�� | ��������ɫ�������ʢ��KSCN��Һ���ձ��� | �����ܽ⣬��Һ��Ѫ��ɫ |
| C | ʵ������ȡ���ռ�����NH3 | ����NH4Cl���壬���������ſ������ռ�����ʪ��ĺ�ɫʯ����ֽ����ƿ�� | NH4Cl�������٣�ʪ��ĺ�ɫʯ����ֽ����ɫ |
| D | ��֤�����ԣ�Fe3+��Cu2+ | ��һ����ͭ�ۼӵ�ʢ��һ�������1.0mol•L-1Fe2��SO4��3��Һ���Թ��� | ͭ���ܽ⣬��Һ����ɫ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com