
| A、硒化氢是无色、有毒、比硫化氢稳定的气体 |
| B、硫酸锶难溶于水,但同硫酸钡一样易溶于盐酸 |
| C、铯的金属性比钠、钾等强,与氧气反应可生成复杂氧化物 |
| D、砹单质是一种有色固体,砹化氢很不稳定,砹化银是难溶于水的白色沉淀 |


科目:高中化学 来源: 题型:
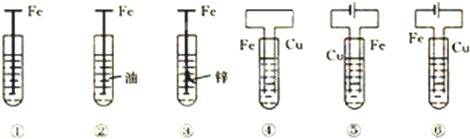
| A、①发生析氢腐蚀 |
| B、③是牺牲阳极的阴极保护法 |
| C、若将⑥的Cu极换成不溶性电极,则⑥是外加电流的阴极保护法 |
| D、腐蚀快到慢的顺序为⑤>④>①>②>③>⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、左池电极反应式:X4++2e-=X2+ |
| B、每消耗1mol Y2O72-,转移3mol电子 |
| C、左池中阴离子数目增加 |
| D、改变右池溶液的c(H+),电流强度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、可用KMnO4酸性溶液检测上述反应是否有阿魏酸生成 |
| B、香兰素、阿魏酸均可与NaHCO3、NaOH溶液反应 |
| C、通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应 |
| D、与香兰素互为同分异构体,分子中有4种不同化学环境的氢,且能发生银镜反应的酚类化合物共有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在周期表中,族序数都等于该族元素的最外层电子数 |
| B、碱金属随原子序数的增大,其熔沸点逐渐降低;卤素单质随原子序数的增大,其熔沸点逐渐升高 |
| C、同周期的主族元素从左到右原子半径逐渐减小,它们形成简单的离子半径逐渐增大 |
| D、非金属性最强的元素,其最高价氧化物对应水化物的酸性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 向等体积等物质的量浓度的H2S和SO2的水溶液各两份中,分别通入Cl2和O2,一段时间后,如图表示通入的气体的量与溶液pH关系的曲线图,下列说法中正确的是( )
向等体积等物质的量浓度的H2S和SO2的水溶液各两份中,分别通入Cl2和O2,一段时间后,如图表示通入的气体的量与溶液pH关系的曲线图,下列说法中正确的是( )| A、曲线a表示向H2S水溶液中通入O2 |
| B、曲线b表示向SO2水溶液中通入O2 |
| C、曲线c表示向SO2水溶液中通入Cl2 |
| D、曲线d表示向H2S水溶液中通入Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(a+3b) mol | ||
B、
| ||
C、
| ||
| D、(cV-3a-9b) mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④ | B、①③ | C、②④ | D、③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com