
| 催化剂 |
| A.更换高效催化剂 | B.增大CO的浓度 |
| C.降低温度 | D.增大压强 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:多选题
| A.NaOH固体 | B.醋酸钠固体 | C.AgNO3溶液 | D.H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.化学反应速率只能用反应物浓度的减少量表示 |
| B.只有温度和催化剂才能影响化学反应速率 |
| C.化学平衡状态指的是反应物和生成物浓度相等时的状态 |
| D.催化剂既能改变正反应的反应速率,又能改变逆反应的反应速率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2(g)的消耗速率与HI(g)的生成速率之比为2:1 |
| B.反应进行的净速率是正、逆反应速率之差 |
| C.正、逆反应速率的比值是恒定的 |
| D.达到平衡时,给体系加压,正、逆反应速度都不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在硫化氢水溶液中加入碱有利于S2-的生成 |
| B.热的纯碱溶液去污能力强 |
| C.高压有利于合成氨反应 |
| D.500℃左右比室温更利于合成氨反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| CaAl2Si2O8 | + | Mg2SiO4 | ? | CaMg2Al2Si3O12 | |
| (钙长石) | (镁橄榄石) | (钙镁)石榴子石 | |||
| 摩尔质量(g/mol) | 278 | 140.6 | 413.6 | ||
| 密度(g/cm3) | 2.70 | 3.22 | 3.50 |
| A.钙长石生成 | B.镁橄榄石生成 |
| C.钙长石和镁橄榄石共存 | D.(钙镁)石榴子石生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| CO2 | H2 | CO | H2O | |
| 甲 | a mol | a mol | 0 mol | 0 mol |
| 乙 | 2a mol | a mol | 0 mol | 0 mol |
| 丙 | 0 mol | 0 mol | 2a mol | 2a mol |
| 丁 | a mol | 0 mol | a mol | a mol |
| A.丙>乙=丁>甲 | B.乙>丁>甲>丙 |
| C.乙=丁>丙=甲 | D.丁>丙>乙>甲 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)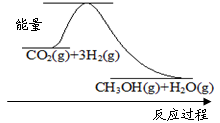
 CH3OH(g)+H2O(g)已达到平衡的是 (单选)。
CH3OH(g)+H2O(g)已达到平衡的是 (单选)。| A.恒温、恒容条件下,容器内的压强不发生变化 |
| B.一定条件下,CH3OH消耗的速率和CH3OH生成的速率相等 |
| C.一定条件下,H2O(g)的浓度保持不变 |
| D.一定条件下,单位时间内消耗1 mol CO2,同时生成1 mol CH3OH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
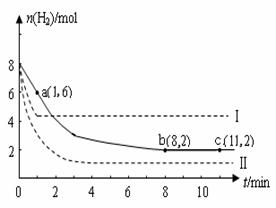
 CH3OH(g),其他条件不变,在300 ℃和500 ℃时,甲醇物质的量n(CH3OH)反应时间t的变化曲线如图所示,下列说法正确的是( )
CH3OH(g),其他条件不变,在300 ℃和500 ℃时,甲醇物质的量n(CH3OH)反应时间t的变化曲线如图所示,下列说法正确的是( )| A.该反应的ΔH>0 |
B.其他条件不变,升高温度反应的平衡常数增大 |
C.300 ℃时,0~t1 min内 CH3OH的平均生成速率为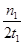 mol·L-1·min-1 mol·L-1·min-1 |
D.A点的反应体系从300 ℃升高到500 ℃,达到平衡时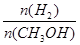 减小 减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com