
下列选项中所涉及的两个量一定相等的是
A.11.2 L Cl2与4.25 g NH3所含有的原子数
B.等质量的Al分别与足量的盐酸、NaOH溶液反应转移的电子数
C.标准状况下36 g H2O与1.204×1024个O2分子所占的体积
D.18.0 g重水(D2O)与20 g Ne所含有的电子数
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源:2015-2016学年浙江省杭州地区七校高一上学期期中联考化学试卷(解析版) 题型:实验题
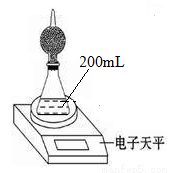
如图是测定铝粉(含铜粉等杂质不与酸反应)的纯度的实验装置。装置为干燥管和锥形瓶,干燥管内装有氯化钙,锥形瓶内所用的硫酸(足量)的物质的量浓度为4mol·L-1。
不同时间电子天平的读数如下表所示:
实验操作 | t/min | 电子天平的读数/g |
装置+硫酸溶液 | 320.0 | |
装置+硫酸溶液+样品 | 0 | 335.0 |
1 | 334.5 | |
2 | 334.1 | |
3 | 333.8 | |
4 | 333.8 |
(1)反应中生成气体的质量为 。
(2)试计算样品中铝的质量分数?(写出计算过程)
(3)求反应后锥形瓶内硫酸溶液(溶液的体积变化忽略)的物质的量的浓度? (写出计算过程)
查看答案和解析>>
科目:高中化学 来源:2016届广东省、潮州金中高三上学期期中联考理综化学试卷(解析版) 题型:填空题
锌是一种应用广泛的金属,目前工业上主要采用“湿法”工艺冶炼锌。某含锌矿的主要成分为ZnS(还含少量FeS等其他成分),以其为原料冶炼锌的工艺流程如图所示:
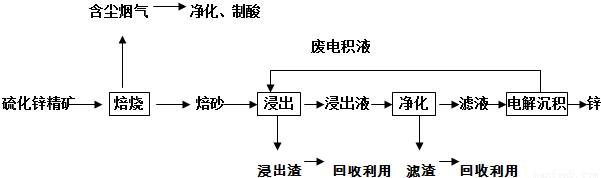
回答下列问题:
(1)硫化锌精矿的焙烧在氧气气氛的沸腾炉中进行,所产生焙砂的主要成分的化学式为 。
(2)焙烧过程中产生的含尘烟气可净化制酸,该酸可用于后续的_______操作。
(3)浸出液“净化”过程中加入的主要物质为锌粉,其作用是__________________,反应的离子方程式为 。
(4)电解沉积过程中的阴极采用铝板,阳极采用Pb-Ag合金惰性电极,阳极逸出的气体是 。
(5)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质。“氧压酸浸”中发生的主要反应的离子方程式为________。
(6)我国古代曾采用“火法”工艺冶炼锌。明代宋应星著的《天工开物》中有关于 “升炼倭铅”的记载:“炉甘石十斤,装载入一泥罐内,……,然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,……,冷淀,毁罐取出,……,即倭铅也。”该炼锌工艺过程主要反应的化学方程式为 。(注:炉甘石的主要成分为碳酸锌,倭铅是指金属锌,碳生成CO)
查看答案和解析>>
科目:高中化学 来源:2016届江西省新余、 万载、宜春三校高三上学期10月联考化学试卷(解析版) 题型:选择题
现有KCl和KBr的混合物3.87 g,将混合物全部溶于水,并加入过量的AgNO3溶液,充分反应后产生6.63 g沉淀物,则原混合物中钾元素的质量分数为
A.24.1% B.25.9% C.40.3% D.48.1%
查看答案和解析>>
科目:高中化学 来源:2016届江西省新余、 万载、宜春三校高三上学期10月联考化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的数值,下列说法正确的是
A.0.1 mol Na2O2中含有的阴离子数为0.2NA
B.标准状况下,由H2O2制得2.24LO2转移的电子数目为0.4NA
C.常温下,1 L pH=2的H2SO4溶液中含有的H+数目为0.02NA
D.常温常压下,8gO3含有4 NA个电子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江铁人中学高一上第一阶段测化学卷(解析版) 题型:计算题
(4分)
(1)5.3g Na2CO3的物质的量为____________,将其配成500mL溶液,所得溶液中Na2CO3的物质的量浓度为____________。取出该溶液10mL,在取出的溶液中通入HCl气体到不再产生气泡为止,共消耗____________mL HCl气体(标准状况)。
(2)V mL Al2(SO4)3溶液中,含有Al 3+ m g,则溶液中SO42-的物质的量浓度为_______。(用含有m、V的式子表示)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江铁人中学高一上第一阶段测化学卷(解析版) 题型:选择题
在NaCl和Na2SO4的混合液中,当Cl—的物质的量浓度是Na+的物质的量浓度的0.6倍时,下列叙述正确的是
A.溶液中可能含有0.5mol Na2SO4和1.5molNaCl
B.SO42-离子和Cl-离子的物质的量之和等于Na+的物质的量
C.SO42-所带的电荷数是Na+所带的电荷数的3/5倍
D.Na2SO4和NaCl物质的量浓度之比为1:3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上第一次月考化学试卷(解析版) 题型:实验题
(12分)某同学预设计实验测定H2在通常状况下的摩尔体积,设计如下实验步骤:①连接如图所示装置,并检查装置的气密性
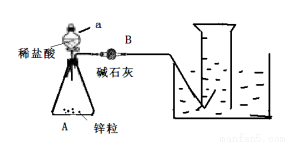
②向a仪器中装入VmL稀盐酸,锥形瓶中加入锌粒,B中加入碱石灰;
③称取A装置和B仪器和药品的总质量,记为a g;
④采取措施使装置A中发生反应;
⑤反应停止后,测得在通常状况下收集的气体体积为b mL;
⑥再次称量A装置和B仪器得总质量(含内装物质),记为c g;
⑦处理数据等。
(1)写出A仪器中发生反应的化学方程式
(2)写出检查该装置气密性的方法
(3)A装置中仪器a的名称为
(4)若拆除B仪器(其他仪器不变), (填“会”或“不会”) 对本实验产生影响,理由是
(5)根据上述数据,计算在通常状况下,H2的摩尔体积Vm= (用含a、b、c等字母的代数式表示)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江嘉兴一中高一上10月阶段测化学卷 (解析版) 题型:选择题
2.16g X2O5中含有0.1mol氧原子,则X的相对原子质量为
A.21.6 B.28 C.14 D.31
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com