

 .
. +NaHCO3→
+NaHCO3→ +H2O+CO2↑.
+H2O+CO2↑. 分析 由图中官能团变化可知,①中只有-COOH转化为-COONa,则需要试剂为碳酸氢钠,②中酚-OH转化为酚钠,则需要试剂为碳酸钠或NaOH,③中醇-OH转化为-ONa,需要试剂为Na,④中酚钠转化为酚,需要试剂为二氧化碳,以此来解答.
解答 解:由图中官能团变化可知,①中只有-COOH转化为-COONa,则需要试剂为碳酸氢钠,②中酚-OH转化为酚钠,则需要试剂为碳酸钠或NaOH,③中醇-OH转化为-ONa,需要试剂为Na,④中酚钠转化为酚,需要试剂为二氧化碳,
(1)由上述分析可知,①中试剂为NaHCO3,②中试剂为NaOH或Na2CO3,③中试剂为Na,④中试剂为CO2(H2O),
故答案为:NaHCO3;NaOH或Na2CO3;Na;CO2(H2O);
(2)①中只有-COOH转化为-COONa,可知A为 ,故答案为:
,故答案为: ;
;
(3)①反应生成A的化学方程式为 +NaHCO3→
+NaHCO3→ +H2O+CO2↑,故答案为:
+H2O+CO2↑,故答案为: +NaHCO3→
+NaHCO3→ +H2O+CO2↑.
+H2O+CO2↑.
点评 本题考查有机物的推断及结构与性质,为高频考点,把握官能团的变化、发生的反应为解答本题关键,侧重分析与应用能力的考查,注意酚、醇、羧酸性质的应用,题目难度不大.


科目:高中化学 来源: 题型:推断题
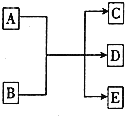 在一定条件下,物质A~E的转化关系如图所示,其中A为单质,常温下E为无色液体.
在一定条件下,物质A~E的转化关系如图所示,其中A为单质,常温下E为无色液体.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4NO3 | B. | NH4Cl | C. | (NH4)2SO4 | D. | NH4HCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 金属阳离子的半径大于它的原子半径 | |
| B. | 金属阳离子的半径小于它的原子半径 | |
| C. | 非金属阴离子的半径小于其原子半径 | |
| D. | 核外电子排布相同的不同微粒,核电荷数越大半径越小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 操作 | 现象 |
| 取适量漂粉精固体,加入100mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝,后褪色 |
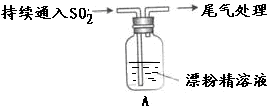 | 液面上方出现白雾; 稍后,出现浑浊,溶液变为黄绿色; 稍后,产生大量白色沉淀,黄绿色褪去 |
| 滴定次数 | 1 | 2 | 3 |
| KI溶液体积/mL | 19.98 | 20.02 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高氯酸(HClO4)的酸性比硫酸强 | B. | 次氯酸的氧化性比稀硫酸强 | ||
| C. | 氯化氢比硫化氢的热稳定性好 | D. | 硫离子还原性比氯离子还原性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有机化合物主要来自自然界众多的有机体 | |
| B. | 可以人工合成 | |
| C. | 有机物分子中的碳原子成键方式具有多样性 | |
| D. | 可以由无机物进行转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子的核外电子排布呈周期性变化 | B. | 原子半径呈周期性变化 | ||
| C. | 原子的电子层数呈周期性变化 | D. | 化合价呈周期性变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com