
 2NH3(g),使1 mol的N
2NH3(g),使1 mol的N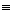 N键断裂吸收946 kJ的能量,使3 mol H—H键断裂共需吸收436 kJ·mol-1×3 mol="1308" kJ的能量,因此使1 mol N2(g)和3 mol H2(g)反应物的化学键断裂共需吸收的能量为946 kJ+1308 kJ="2254" kJ。而2 mol NH3(g)中含6 mol N—H键,形成6 mol N—H键时放出能量为391 kJ·mol-1×6 mol="2346" kJ。因此反应热应等于生成物分子形成时所释放的总能量(2346 kJ·mol-1)与反应物分子断裂时所吸收的总能量(2254 kJ·mol-1)的差,即放出了92 kJ·mol-1的能量,ΔH="-92" kJ·mol-1。
N键断裂吸收946 kJ的能量,使3 mol H—H键断裂共需吸收436 kJ·mol-1×3 mol="1308" kJ的能量,因此使1 mol N2(g)和3 mol H2(g)反应物的化学键断裂共需吸收的能量为946 kJ+1308 kJ="2254" kJ。而2 mol NH3(g)中含6 mol N—H键,形成6 mol N—H键时放出能量为391 kJ·mol-1×6 mol="2346" kJ。因此反应热应等于生成物分子形成时所释放的总能量(2346 kJ·mol-1)与反应物分子断裂时所吸收的总能量(2254 kJ·mol-1)的差,即放出了92 kJ·mol-1的能量,ΔH="-92" kJ·mol-1。

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.Q2=Q1=197kJ | B.Q1<Q2<197kJ | C.Q2<Q1<197kJ | D.Q1=Q2<197kJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Q1=Q2 | B.Q1>Q2 | C.Q1<Q2 | D.无法判断 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
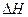 的绝对值均正确)
的绝对值均正确)| A.C2H5OH(l)+3O2(g)==2CO2(g)+3H2O(g);△H=—1367.0 kJ/mol(燃烧热) |
| B.NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l);△H=+57.3kJ/mol(中和热) |
| C.S(s)+O2(g)===SO2(g);△H=—269.8kJ/mol(反应热) |
| D.2NO2==O2+2NO;△H=+116.2kJ/mol(反应热) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com