
【题目】密闭容器内有四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表所示,下列说法正确的是( )
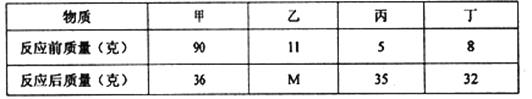
A. 该反应是化合反应 B. M的值是15
C. 反应中甲、丙质量比为15:27 D. 该反应是分解反应
科目:高中化学 来源: 题型:
【题目】按照无机物的分类方法,下列各组物质中,属于不同类型的物质是( )
A.火碱、烧碱、生石灰
B.生石灰、冰、干冰
C.熟石灰、苛性钠、氢氧化钾
D.纯碱、硫酸钠、胆矾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成具有良好生物降解性的有机高分子材料是有机化学研究的重要课题之一。聚醋酸乙烯酯(PVAc)水解生成的聚乙烯醇(PVA),具有良好生物降解性,常用于生产安全玻璃夹层材料PVB。有关合成路线如下图(部分反应条件和产物略去)。


回答下列问题:
(1)A为饱和一元醇,其氧的质量分数约为34.8%,A的化学名称为___________,PVA的结构简式为_________________。
(2)C中官能团的名称是_________________,A~F中核磁共振氢谱出峰最多的是______(填代号)。
(3)反应①包含的反应类型是_________________;反应④的化学方程式为__________________。
(4)PVAc是由F加聚而成,与F具有相同官能团的同分异构体还有___________种;写出其中一种的结构简式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)2molCO与3molCO2的质量之比________;分子数之比为_______ ;含氧原子的数目之比为______。
(2)有下列物质①6gH2;②2molNH3;③4℃时9mL水(水的密度1g/mL);④1.204×1023个硫酸分子;⑤标准状况下,5.6L二氧化碳。分子数由少到多的顺序是_____________,质量由小到大的顺序是______________(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有m g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1,若阿伏加德罗常数用NA表示。
①该气体的物质的量为________mol。
②该气体所含原子总数为________个。
③该气体在标准状况下的体积为________
(2)已知有C2H4O、C3H6 O、C4H8 O三种物质的混合物,测得氧元素的质量分数为32%,则混合物中C元素的质量分数为___________________________________________,则混合物中H元素的质量分数为_________________________(保留一位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaCO3与稀盐酸反应生成CO2的量与反应时间的关系如图所示。下列结论不正确的是
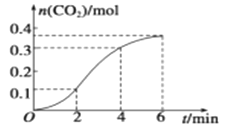
A. 反应在2~4 min内平均反应速率最大
B. 反应开始4 min内温度比浓度对反应速率的影响大
C. 4 min后,反应速率减小的主要原因是c(H+)减小
D. 反应在2~4 min内生成CO2的平均反应速率为v(CO2)=0.1 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(ClNO)常用作催化剂和合成洗涤剂,其沸点为-5.5℃,易水解。某学习小组在实验室中用下图所示装置制备ClNO。已知:HNO2既有氧化性又有还原性;AgNO2微于水,能溶于硝酸,AgNO2+HNO3=AgNO3+HNO2。
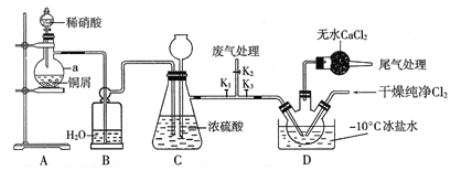
回答下列问题:
(1)仪器a的名称为_____________,装置B的作用是____________。
(2)装置C中长颈漏斗的作用是____________。
(3)实验开始时,先打开K1、K2,关闭K3,再打开分液漏斗活塞滴人适量稀硝酸,当观察到C中______时关闭K1、K2。向装置D三颈瓶中通人千燥纯净Cl2,当瓶中充满黄绿色气体时,再打开K1、K3,制备ClNO。
(4)装置D中干燥管的作用是__________________。
(5)实验过程中,若学习小组同学用酒精灯大火加热制取NO,对本实验造成的不利影响是____、________。
(6)ClNO与H2O反应生成HNO2和HCl。
①设计实验证明HNO2是弱酸________________。(仅提供的试剂:1mol/L盐酸、1mol/L HNO2、Na、NaNO2溶液、红色石蕊试纸、蓝色石蕊试纸)
②要验证ClNO与H2O反应后的溶液中存在Cl-和HNO2,合理的操作步骤及正确的顺序是_____(填序号)。
a.向烧杯中滴加过量KI淀粉溶液,溶液变蓝色
b.取1.0mL三颈瓶中产品于烧杯中,加入10.0mLH2O充分反应
c.向烧杯中滴加酸性KMnO4溶液,溶液紫色褪去
d.向烧杯中滴加足量AgNO3溶液,有白色沉淀生成,加入稀硝酸,搅拌,仍有白色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com