
【题目】合成氨工业对国民经济和社会发展具有重要意义。对于密闭容器中的反应:N2(g)+3H2(g)![]() 2NH3(g),在673 K、30 MPa下,n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述正确的是
2NH3(g),在673 K、30 MPa下,n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述正确的是

A. 点a的正反应速率比点b的小
B. 点c处反应达到平衡
C. 点d(t1时刻)和点e(t2时刻)处n(N2)不一样
D. 点e处反应达到平衡
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一新型、高效、无毒的多功能水处理剂。制备K2FeO4如下图:查阅资料:K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
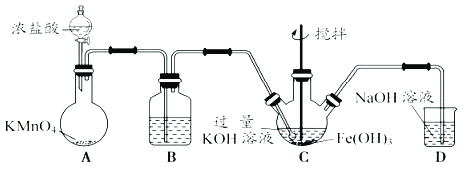
(1)A为制取氯气发生装置,其中盛放浓盐酸的仪器名称为______,A中化学反应的还原剂是______。
(2)装置B的作用是除杂,所用试剂为___________。
(3)C为制备K2FeO4装置,KOH溶液过量的原因是_________________________。
(4)D为尾气处理装置,发生反应的离子方程式为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以N2和H2为反应物,盐酸酸化的NH4Cl溶液为电解质的原电池,工作原理如下图所示,下列说法不正确的是

A. b电极为负极
B. 反应过程中,溶液中的Cl-向a电极移动
C. a电极的电极反应式为:N2+6e-+8H+=2NH4+
D. 电池反应为N2+3H2+2HCl=2NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应现象中,叙述正确的是
A.灼热的铁丝在氯气中燃烧,集气瓶内产生棕黄色烟雾
B.氢气在氯气中燃烧,集气瓶口有白雾
C.钠在氯气中燃烧,集气瓶内产生大量的白雾
D.灼热的铜丝在氯气中燃烧,集气瓶内产生红棕色烟
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. NO2、SO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8e-稳定结构;
B. P4和CH4都是正四面体分子且键角都为109o28ˊ;
C. CO2、SO2都是直线形的分子
D. CH2=CH2分子中共有五个σ键和一个π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苏丹红一号(sudan Ⅰ)是一种偶氮染料,不能作为食品添加剂使用。它是由苯胺和2-萘酚为主要原料制备的,它们的结构简式如下所示:

![]()

(苏丹红一号) (苯胺) (2-萘酚)
(提示: 可表示为
可表示为![]() )
)
(1)苏丹红一号的化学式(分子式)为______。
(2)在下面化合物(A)~(D)中,与2-萘酚互为同分异构体的有(填字母代号)_____。




(A) (B) (C) (D)
(3)上述化合物(C)含有的官能团是_____。
(4)在适当的条件下,2-萘酚经反应可得到芳香化合物E(C8H6O4),1molE与适量的碳酸氢钠溶液反应可放出二氧化碳44.8L(标准状况),E与溴在有催化剂存在时反应只能生成两种一溴代物,两种一溴代物的结构简式分别是______________________________,E与碳酸氢钠反应的化学方程式是____________________。
(5)若将E与足量乙醇在浓硫酸作用下加热,可以生成一个化学式(分子式)为C12H14O4的新化合物,该反应的化学方程式是____________________,反应类型是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某硅酸盐研究所在硅酸盐材料和闪烁晶体等领域研究上取得了重大的成就。
(1)[SiO4]4-是构成硅酸盐的基本结构单元,通过共用氧相连可形成硅氧组群。
①基态硅原子价电子的轨道表示式是_____________。
②与[SiO4]4-互为等电子体的微粒符号是_____________任写一种)。
③下图为一种硅氧组群的结构示意图,其离子符号为_____________,其中Si原子的杂化方式为_____________。

④电负性:Si ______O (填“>”、 “=”或“<” )。
(2)钨酸铅(PWO)是一种闪烁晶体,晶胞结构如图所示。

①PWO中钨酸根结构式为 ,该离子中,σ键和π键的个数比是_____________。
,该离子中,σ键和π键的个数比是_____________。
②PWO晶体中含有的微粒间作用力是_____________ (填标号)。
A.范德华力 B.离子键 C.共价键 D.金属键
③己知PWO的摩尔质量为Mg·mol-1,则该晶体的密度d=_____________g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
Ⅰ、下列涉及有机化合物的说法是正确的是 ______________________
A.除去乙烷中少量的乙烯:通过酸性KMnO4溶液进行分离
B.甲苯硝化制对硝基甲苯与苯甲酸和乙醇反应制苯甲酸乙酯的反应类型不同
C.用氢氧化钠溶液鉴别花生油和汽油
D.除去乙醇中少量的乙酸:加足量生石灰,蒸馏
E.除去乙酸乙酯中少量的乙酸:用饱和氢氧化钠溶液洗涤、分液、干燥、蒸馏
Ⅱ、正丁醛经催化加氢得到含少量正丁醛的1-丁醇粗品,为纯化1-丁醇,该小组查阅文献得知:①R-CHO+NaHSO3(饱和)→RCH(OH)SO3Na↓;
②沸点:乙醚34℃,1-丁醇118℃,并设计出如下提纯路线:
![]()
(1)试剂1为__________,操作2为__________,操作3为__________.
(2)写出正丁醛银镜反应方程式___________________________________
Ⅲ、已知:1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度是2.18克/厘米3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验中可以用下图所示装置制备1,2-二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水,溴蒸汽有毒)。请填写下列空白:

(1)写出制备1,2-二溴乙烷的化学方程式: ________________________________。
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象:_______________________________________。
(3)c装置内NaOH溶液的作用是______________________________;
(4)e装置内NaOH溶液的作用是_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com