
科目:高中化学 来源:2015-2016学年湖北省宜昌市高二下期中化学试卷(解析版) 题型:填空题
I .(1)同温同压下,物质的量为2:3的SO2气体和SO3气体,其原子个数之比为 ,气体密度之比为 。相同质量的SO2气体和SO3气体,其分子数之比为
(2)在同温、同压下,实验测得CO、N2和O2三种气体的混合气体的密度是H2的14.5倍,其中O2的质量分数为 .
II.Fe(OH)3胶体可使水中悬浮物凝聚沉淀,是城市饮用水处理新技术.
(1)实验室制取Fe(OH)3 相应的离子方程式是 .
(2)氢氧化铁胶体还可以和次氯酸钠在碱性介质中反应得到铁酸钠Na2FeO4,铁酸钠具有强氧化性从而对来自河湖的淡水的进行消毒,请给下列方程式配平
Fe3++ ClO﹣+ OH-﹣= FeO42-﹣+ Cl-﹣+ H2O.
III(1)已知TiCl4在通常情况下是无色液体,熔点为-37℃,沸点为136℃;TiCl4在潮湿空气中易水解产生白雾,同时产生H2TiO3固体.写出TiCl4在潮湿空气中水解的化学方程式是_________________
(2) 已知TiO2+2Cl2+2C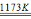 TiCl4+2CO ,TiCl2、Cl2和C反应制得的TiCl4最好的提纯方法是__________(填操作名称)。
TiCl4+2CO ,TiCl2、Cl2和C反应制得的TiCl4最好的提纯方法是__________(填操作名称)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省襄阳市高一5月月考化学试卷(解析版) 题型:选择题
某航空站安装了一台燃料电池,该电池可同时提供电和水蒸气,所用燃料为氢气,电解质为熔融的碳酸钾。已知电池的总反应为2H2+O2=2H2O,正极反应为O2+2CO2+4e?=2CO32?。下列说法正确的是( )
A.该电池可在常温或高温时工作,对环境有较强的适应性
B.负极反应为H2+2OH?-2e?=2H2O
C.该电池工作时负极有CO2生成
D.该电池供应2molH2O,同时转移2mol电子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下期中化学试卷(解析版) 题型:选择题
对于反应A2+3B2===2C来说,以下化学反应速率的表示中,反应速率最快的是( )
A.v(B2)=0.8 mol/(L·s) B.v(A2)=0.5 mol/(L·s)
C.v(C)=0.6 mol/(L·s) D.v(B2)=1.2 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下期中化学试卷(解析版) 题型:选择题
下列各组物质中化学键的类型相同的是( )
A.HCl MgCl2 NH4Cl B.H2O Na2O CO2
C.CaCl2 NaOH H2S D.NH3 H2O CO2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省徐州市高二下第二次质量检测化学试卷(解析版) 题型:填空题
已知Q、R、X、Y、Z、W都是周期表中前四周期的元素,它们的核电荷数依次增大,其中Q原子外层电子数是内层电子数的两倍;化合物R2Z的晶体为离子晶体,Z原子核外的M层中有两对成对电子;X元素最外层电子数与最内层电子数相同;Y单质的晶体类型在同周期的单质中没有相同的;W元素所在族有三列,只有两个未成对的电子。请根据以上信息,回答下列问题:(答题时,Q、R、X、Y、Z、W用所对应的元素符号表示)
(1)W的外围电子(价电子)排布式是 。
(2)Q、R、X、Y的第一电离能由小到大的顺序为_ 。(用元素符号表示)
(3)QZ2分子的空间构型为 形。
(4)R的氯化物的熔点比Y的氯化物的熔点_ _(填高或低),理由是_ _ 。
(5)据报道,只含Q、X、W三种元素的晶体竟然具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构如图,试写出该晶体的化学式_ 。晶体中每个X原子周围距离最近的W原子有__ _个。
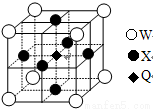
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省徐州市高二下第二次质量检测化学试卷(解析版) 题型:选择题
ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O下列说法正确的是( )
A.KClO3在反应中得到电子
B.ClO2是氧化产物
C.H2C2O4在反应中被氧化
D.1 mol KClO3参加反应,有2 mol电子转移
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省江阴市高二下期中化学试卷(解析版) 题型:填空题
将2molSO2和1molO2混合置于体积可变,压强恒定的密闭容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)  2SO3(g);△H﹤0,当反应进行到时间t1点时达到平衡状态,测得混合气体总物质的量为2.1 mol。试回答下列问题:
2SO3(g);△H﹤0,当反应进行到时间t1点时达到平衡状态,测得混合气体总物质的量为2.1 mol。试回答下列问题:
(1)写出该反应的平衡常数表达式:K =
(2)反应进行到t1时,SO2的体积分数为 ;
(3)若在t1时充入一定量的氩气(Ar),SO2的物质的量将 (填“增大”、“减小”或“不变”);
(4)若在t1时升温,重新达到平衡状态,新平衡混合物中气体的总物质的量 2.1mol(填“<”、“>”或“=”),简单说明原因 ;
(5)若其它条件不变,在t1时再加入0.2molSO2、0.1molO2 和1.8molSO3,在图中作出从t0→t1→t2点这段时间内SO2的物质的量变化曲线。
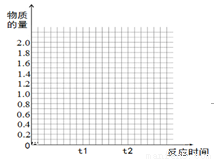
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆石河子二中高一下学期第二次月考化学试卷(解析版) 题型:选择题
将铜棒和锌棒用导线连接后插入稀硫酸溶液中,下列叙述中正确的是( )
A.该装置能形成原电池,其中锌是负极
B.该装置能形成原电池,其中铜是负极
C.该装置不能形成原电池
D.以上说法均不正确
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com