
有A、B、C三种可溶性正盐,阴、阳离子各不相同,其阴离子的摩尔质量依次增大(按A、B、C的顺序),将等物质的量的A、B、C溶于水,所得溶液中只含有Fe3+、K+、SO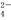 、NO
、NO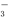 、C
、C l-五种离子,同时生成一种白色沉淀。
l-五种离子,同时生成一种白色沉淀。
请回答下列问题:
(1)经检验,三种正盐中还含有下列选项中的一种离子,该离子是 。
A.Na+ B.Mg2+ C.Cu2+ D.Ag+
(2)三种正盐的化学式分别是:A ,B ,C 。
(3)若将A、B、C三种正盐按一定比例溶于水后,所得溶液中只含有Fe3+、SO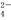 、NO
、NO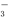 、K+四种离子且物质的量之比依次为1∶2∶3∶4,则A、B、C三种正盐的物质的量之比为 。
、K+四种离子且物质的量之比依次为1∶2∶3∶4,则A、B、C三种正盐的物质的量之比为 。
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源:2016-2017学年河北省高二上第三次月考化学卷(解析版) 题型:选择题
已知,常温下某浓度NaHSO3稀溶液的pH<7,则该稀溶液中下列粒子关系正确的是
A.c(Na+)>c(HSO3-)>c(H2SO3)>c(SO32-)
B.c(Na+)>c(HSO3-)+c(SO32-)
C.c(Na+)+c(H+)=2c(SO32-)
D.c(Na+)+c(H+)=c(HSO3-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源:2017届安徽省等四校高三上10月联考化学试卷(解析版) 题型:选择题
下列反应的离子方程式书写正确的是
A.NaAlO2溶液中通入过量的CO2: 2AlO2-+3H2O+CO2=2Al(OH)3↓+CO32-
B.向海带灰浸出液中加入稀硫酸、双氧水:2I-+2H++H2O2=I2+ 2H2O
C.磨口玻璃试剂瓶被烧碱溶液腐蚀:SiO2+2Na++2OH-=Na2SiO3↓+H2O
D.NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3-+ OH-+ Ba2+=H2O+BaCO3↓
查看答案和解析>>
科目:高中化学 来源:2017届内蒙古高三上9月月考化学卷(解析版) 题型:推断题
富马酸(反式丁烯二酸)与Fe2+形成的配合物——富马酸铁又称“富血铁”,可用于治疗缺铁性贫血。以下是合成富马酸铁的一种工艺路线:

回答下列问题:
(1)A的化学名称为 ,由A生成B的反应类型为 。
(2)C的结构简式为 。
(3)富马酸的结构简式为 。
(4)检验富血铁中是否含有Fe3+的实验操作步骤是 。
(5)富马酸为二元羧酸,1mol富马酸与足量饱和NaHCO3溶液反应可放出 L CO2
(标况);富马酸的同分异构体中,同为二元羧酸的还有 、 (写出结构简式)
查看答案和解析>>
科目:高中化学 来源:2017届内蒙古高三上9月月考化学卷(解析版) 题型:选择题
若4.8 g某金属与足量盐酸充分反应,放出4.48 L(标准状况)H2,则该金属是( )
A.Al B.Mg C.Fe D.Zn
查看答案和解析>>
科目:高中化学 来源:2017届内蒙古高三上9月月考化学卷(解析版) 题型:选择题
由铝屑与盐酸、氢氧化钠溶液反应制取10 mol Al(OH)3,最少需要消耗HC1和NaOH的物质的量为( )
A.30 mol、30 mol B.10 mol、10 mol
C.7.5 mol、7.5 mol D.2.5 mol、2.5 mol
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上学期第二次段考化学试卷(解析版) 题型:推断题
氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末;微溶于水、不溶于乙醇及稀硫酸;在空气中迅速被氧化成绿色;见光则分解,变成褐色.如图是工业上以制作印刷电路板的废液(含Fe3+、Cu2+、Fe2+、Cl﹣)生产CuCl的流程:
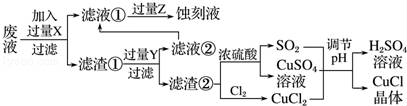
根据以上信息回答下列问题:
(1)写出生产过程中所加试剂:X ,Y .
(2)生产中为了提高CuCl产品的质量,采用抽滤法快速过滤,析出的CuCl晶体不用水而用无水乙醇 洗涤的目的是 ;生产过程中调节溶液的pH不能过大的原因是 .
洗涤的目的是 ;生产过程中调节溶液的pH不能过大的原因是 .
(3)写出产生CuCl的化学方程式: .
(4)在CuCl的生成过程中除环境问题、安全问题外,还应该注意的关键问题是 。
查看答案和解析>>
科目:高中化学 来源:2017届湖南省益阳市高三上学期第二次月考化学试卷(解析版) 题型:实验题
I.某兴趣小组利用下图装置测定某硫酸工厂排放尾气中二氧化硫的含量,图中气体流量计B用于准确测量通过的尾气体积。将尾气通入一定体积已知浓度的碘水中测定SO2的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。
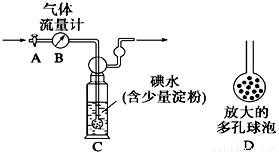
⑴ C中导管末端连接一个多孔球泡D,可以提高实验的准确度,其理由是 。
⑵ C中发生反应的离子方程式 。
⑶ C中溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量 (填“偏高”、“偏低”或“无影响”)。
II.实验室常用Na2SO3固体与浓硫酸反应制取SO2 :
⑷ 现有已制得SO2的饱和溶液,请利用此溶液(其他试剂任选),设计一个简单实验,比较SO2与Fe2+ 还原性的强弱(要求:写出实验步骤、现象和结论) 。
⑸ 某研究小组测定部分变质的Na2SO3固体样品中Na2SO3的含量:
① 取a克Na2SO3固体样品配制成100mL溶液,取10.00mL该溶液于锥形瓶中,加入几滴淀粉溶液作指示剂,0.0100mol/L碘水进行滴定,滴定终点现象为 ,记录数据,重复滴定2次,平均消耗碘水20.00mL。
② 计算:样品中亚硫酸钠的质量分数为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com