
关于反应中的先后顺序,下列评价正确的是
A.向浓度都为0.1 mol/L 的FeCl3和CuCl2混合溶液中加入铁粉,CuCl2首先反应
B.向NH4Al(SO4)2溶液中滴加少量的NaOH溶液,NH4+首先反应
C.向浓度都为0.1 mol/LNa2 CO3和NaOH溶液通入CO2气体,NaOH首先反应
D.向浓度都为0.1 mol/L 的FeCl3加入质量相同、颗粒大小相同的铁和铜,铜首先反应
科目:高中化学 来源: 题型:
已知:2 Zn(s)+O2(g)=2ZnO(s) △H=-701.0kJ·mol-1
Zn(s)+O2(g)=2ZnO(s) △H=-701.0kJ·mol-1
2Hg(l)+O2(g)=2HgO(s) △H=-181.6kJ·mol-1
则反应Zn(s)+ HgO(s)=ZnO(s)+ Hg(l)的△H为
A. +519.4kJ·mol-1 B. +259.7 kJ·mol-1
C. -259.7 kJ·mol-1 D. -519.4kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
有下列各组物质:
A.O2和O3 B.12C和13C C.CH3—CH2—CH2—CH3和(CH3)2CHCH3 D.甲烷和庚烷
E.CH3CH2CH2CH(C2H5)CH3和CH3CH2CH2CH(CH3)C2H5
(1)_________组两物质互为同位素;
(2)_________组两物质互为同素异形体;
(3)_________组两物质属于同系物;
(4)_________组两物质互为同分异构体;
(5)__ _______组中两物质是同一物质
_______组中两物质是同一物质 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
某合作学习小组讨论辨析以下说法:①粗盐和碱石灰都是混合物;②天然气和水煤气都是可再生资源;③冰和水混合物不是混合物而是纯净物;④不锈钢和目前流通的硬币都是合金;⑤盐酸和食醋既是化合物又是酸;⑥纯碱和烧碱都是碱;⑦豆浆和雾都是胶体。上述说法正确的是
A.①③④⑦ B.①②⑤⑥ C.③⑤⑥⑦ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
NA为阿伏伽德罗常数,下列叙 述错误的是
述错误的是
A.标准状况下,11. 2 L氦气中含有0.5 NA原子
2 L氦气中含有0.5 NA原子
B.标准状况下,0.1 mol Cl2参加反应,转移的电子数目一定为0. 2 NA
C.常温常压下,46g NO2和N2O4混合气体中含有原子总数为3NA
D.1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移电子总数NA个
查看答案和解析>>
科目:高中化学 来源: 题型:
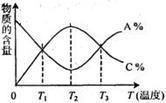
经一定时间后,可逆反应aA+bB  cC中物质的含量A%和C%
cC中物质的含量A%和C%
随温度的变化曲线如右图所示,下列说法正确的是
A.该反应在T1、T3温度时达到化 学平衡
学平衡
B.该反应在T1温度时达到化学平衡
C.该反应为放热反应
D.升高温度,平衡会向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
近年来我国的航天事业取得了巨大的成就,在航天发射时,常用肼(N2H4)及其衍生物作火箭推进剂。
(1)液态肼作火箭燃料时,与液态N2O4混合发生氧化还原反应,已知每克肼充分反应后生成氮气和气态水放出热量为a KJ,试写出该反应的热化学方程式
(2)在实验室中,用N2H4·H2O与NaOH颗粒一起蒸馏,收集114~116℃的馏分即为无水肼。在蒸馏过程中需要的仪器有酒精灯、锥形瓶、冷凝管、牛角管(接液管)、蒸馏烧瓶,除上述必需的仪器外,还缺少的玻璃仪器是
(3)肼能使锅炉内壁的铁锈(主要成分Fe2O3)变成磁性氧化铁(Fe3O4)层,可减缓锅炉锈蚀。若反应过程中肼转化为氮气,则每生成1molFe3O4,需要消耗肼的质量为 g。
(4)磁性氧化铁(Fe3O4)的组成可写成FeO·Fe2O3。某化学实验小组通过实验来探究一黑色粉末是否由Fe3O4、CuO组成(不含有其它黑色物质)。探究过程如下:
提出假设:假设1. 黑色粉末是CuO; 假设2. 黑色粉末是Fe3O4;
假设3. 。
设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂。
①若溶液显蓝色,则假设1成立。
②若所得溶液显血红色,则假设 成立。
③为进一步探究,继续向②所得溶液加入足量铁粉,若有红色固体析出的现象,则假设3成立。
有另一小组同学提出,若混合物中CuO含量较少,可能加入铁粉后实验现象不明显。
查阅资料:Cu2+与足量氨水反应生成深蓝色溶液,Cu2++4NH3·H2O=Cu(NH3)42++4H2O。
④为探究是假设2还是假设3成立,另取少量粉末加稀硫酸充分溶解后,再加入足量氨水,若假设2成立,则产生 现象;若假设3成立,则产生红褐色沉淀,同时溶液呈深蓝色。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上制备BaCl2的工艺流程图如下:
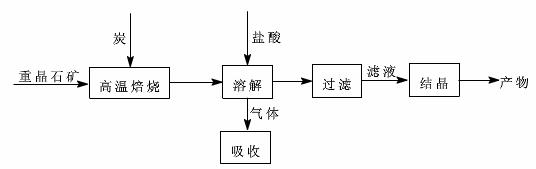
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得
BaSO4(s) + 4C(s)  4CO(g) + BaS(s) △H1 = 571.2
4CO(g) + BaS(s) △H1 = 571.2 kJ·mol-1 ①
kJ·mol-1 ①
BaSO4(s) + 2C(s)  2CO2(g) + BaS(s) △H2= 226.2 kJ·mol-1 ②
2CO2(g) + BaS(s) △H2= 226.2 kJ·mol-1 ②
⑴气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为 。
⑵向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,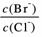 = 。
= 。
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
⑶反应C(s) + CO2(g)  2CO(g)的△H= kJ·mol-1。
2CO(g)的△H= kJ·mol-1。
⑷实际生产中必须加入过量的炭,同时还要通入空气,其目的是 , 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y是主族元素,I为电离能,单位是KJ/mol。根据下表数据判断错误的是( )
| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4600 | 6900 | 9500 |
| Y | 580 | 1800 | 2700 | 11600 |
A.元素X的常见化合价是+1价 B.元素X与氯形成化合物时,化学式可能是XCl
C.元素Y是IIIA族的元素 D.若元素Y处于第3周期,它可与冷水剧烈反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com