
【题目】已知某炔烃与卤素按物质的量为1:2发生加成反应,反应后,生成的有机物至少需6mol的卤素单质才能把生成的有机物中的氢全部取代,则该炔烃可能是( )
A.丙炔
B.1﹣丁炔
C.3﹣己炔
D.2﹣庚炔
科目:高中化学 来源: 题型:
【题目】常温下,在给定的四种溶液中加入以下各种离子,能在原溶液中较大量共存的是( )
A.pH<7的溶液:Cu2+、Na+、Mg2+、 ![]()
B.滴加酚酞溶液显红色的溶液:Fe3+、 ![]() 、Cl、
、Cl、 ![]()
C.所含溶质为NaOH的溶液:K+、 ![]() 、
、 ![]() 、H+
、H+
D.在碱性溶液:K+、 ![]() 、Br、Ba2+
、Br、Ba2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50mL 0.50molL﹣1盐酸与50mL 0.55molL﹣1 NaOH溶液,在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.回答下列问题: 
起始温度t1/℃ | 终止温度t2/℃ | 温度差 | |||
HCl | NaOH | 平均值 | |||
1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
2 | 24.5 | 24.2 | 24.45 | 27.6 | 3.15 |
3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
(1)该实验中,量取50mL盐酸或NaOH溶液,需要用到的玻璃仪器除胶头滴管外还要;
(2)装置中大、小烧杯之间填满碎泡沫塑料的目的是;
(3)某同学实验记录的数据如上表所示,其中记录的终止温度是指温度;
(4)计算该实验发生中和反应时放出的热量为J[中和后生成的溶液的比热容c=4.2J(g℃)﹣1 , 稀溶液的密度都为1gcm﹣3];
(5)若用50mL 0.55molL﹣1的氨水(NH3H2O)代替NaOH溶液进行上述实验,通过测得的反应热来计算中和热,测得的中和热△H会(填“偏大”、“偏大”或“不变”),其原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种化合物,有的是药物,有的是香料.它们的结构简式如图所示: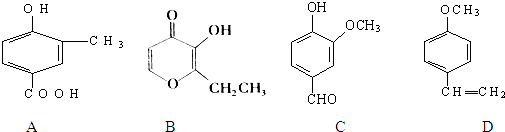
(1)化合物A的分子式是;A中含有的官能团的名称是;
(2)A,B,C,D四种化合物中互为同分异构体的是(填序号);
(3)化合物B的核磁共振氢谱中出现组峰;
(4)在溴水中与溴发生加成反应的是(填序号);与三氯化铁溶液反应呈紫色的是(填序号);1mol D最多能与mol的氢气发生加成反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】综合利用海水可以制备食盐、纯碱、金属镁等钩质,其流程示意图如下: 
(1)在上述反应①~⑤中,没有涉及的化学反应类型是 .
A.分解反应
B.化合反应
C.复分解反应
D.置换反应
(2)写出反应③的离子方程式 .
(3)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下: ①溶解;
②依次加入过量的BaCl2溶液、NaOH溶液、;
③过滤;
④;
⑤蒸发结晶.
其中加入过量氯化钡溶液的目的是 .
(4)X溶液中的主要阳离子是Na+和 .
(5)检验纯碱样品中是否含NaCl应选用的试剂是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分接触(如图),容器内的压强由大到小的顺序是( )
编号 | ① | ② | ③ | ④ |
气体M | H2S | NH3 | HI | NO |
气体N | SO2 | HCl | Cl2 | O2 |
![]()
A.③=④>①>②
B.③>④>①>②
C.④>③>②>①
D.④>③>①>②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com