
【题目】有关物质的转化关系如图所示(部分物质和条件已略去).F是最简单的烃,B是最常见的无色液体,A是一种淡黄色固体,G是一种既能溶于强酸又能溶于强碱的白色固体,C由两种短周期元素组成,其摩尔质量为144gmol﹣1 . 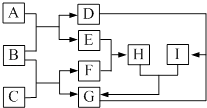
请问答下列问题:
(1)F的电子式为 .
(2)C的化学式为 .
(3)写出A与B反应的化学方程式: .
(4)写出D溶液与G反应的离子方程式: .
【答案】
(1)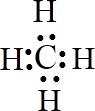
(2)Al4C3
(3)2Na2O2+2H2O=4NaOH+O2↑
(4)Al(OH)3+OH﹣=AlO2﹣+2H2O
【解析】解:F是最简单的烃,则F为CH4 , B是最常见的无色液体,则B为H2O,A是一种淡黄色固体,A能与水反应生成D和E,所以A为Na2O2 , D、E应为O2和NaOH,其中D能与甲烷反应,所以D为NaOH,E为O2 , 氧气与甲烷反应生成H为CO2 , G是一种既能溶于强酸又能溶于强碱的白色固体,I和H反应生成G,则G应为Al(OH)3 , I为NaAlO2 , D与G反应生成偏铝酸钠,符合转化关系,根据元素守恒可知,C由两种短周期元素组成,其摩尔质量为144gmol﹣1 , 所以C为Al4C3 , Al4C3与水反应生成氢氧化铝和甲烷,(1)F为CH4 , F的电子式为 ![]() ,所以答案是:
,所以答案是: ![]() ; (2)根据上面的分析可知,C为Al4C3 , 所以答案是:Al4C3;(3)A与B反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑,所以答案是:2Na2O2+2H2O=4NaOH+O2↑;(4)D为NaOH,G为Al(OH)3 , D溶液与G反应的离子方程式为:Al(OH)3+OH﹣=AlO2﹣+2H2O, 所以答案是:Al(OH)3+OH﹣=AlO2﹣+2H2O;
; (2)根据上面的分析可知,C为Al4C3 , 所以答案是:Al4C3;(3)A与B反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑,所以答案是:2Na2O2+2H2O=4NaOH+O2↑;(4)D为NaOH,G为Al(OH)3 , D溶液与G反应的离子方程式为:Al(OH)3+OH﹣=AlO2﹣+2H2O, 所以答案是:Al(OH)3+OH﹣=AlO2﹣+2H2O;


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
【题目】N2H4是一种高效清洁的火箭燃料,0.25mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5kJ热量.则下列热化学方程式中正确的是( )
A.![]() N2H4(g)+
N2H4(g)+ ![]() O2(g)=
O2(g)= ![]() N2(g)+H2O(g)△H=+267kJmol﹣1
N2(g)+H2O(g)△H=+267kJmol﹣1
B.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=﹣534kJmol﹣1
C.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=+534kJmol﹣1
D.N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=﹣133.5kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质进行一氯取代反应,产物只有两种的是 ( )
A. (CH3)2CHCH(CH3)2 B.(CH3CH2)2CHCH3
C. (CH3)2CHCH2CH2CH3 D.(CH3)3CCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl3溶液与下列物质的反应,其中与Fe3+的水解无关的是 ( )
①紫色石蕊试液 ②碘化钾 ③煮沸的蒸馏水 ④硫化氢 ⑤铜粉 ⑥小苏打溶液
A.①②③④B.②④⑤C.③⑤⑥D.①⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)根据如图金属应用实例推断,金属具有的物理性质有________________(至少答两点)。

(2)厨房中的下列物品所使用的主要材料属于金属材料的是________(填字母)。
A. 陶瓷碗 B. 不锈钢炊具
C. 橡胶手套 D. 铜质水龙头
(3)钙、锌、铁、铜四种金属的活动性顺序由强到弱的顺序是________________(用化学符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属材料在人类的生产、生活中有着十分重要的作用。
(1)多种金属可以压成薄片、抽成细丝,说明金属具有________性。
(2)实验室有打磨过的铝片、铁片和硫酸铜溶液。兴趣小组同学欲验证铝、铁和铜的活动性顺序,进行如下操作:
①取少量硫酸铜溶液于试管A中,将铁片(足量)插入硫酸铜溶液中,充分反应后将铁片取出,观察到的实验现象是_______________________;
②__________________________________(请补充实验具体操作);
③取少量硫酸铜溶液于试管B中,将铝片插入硫酸铜溶液中,充分反应。写出该反应的化学方程式___。结论:三种金属的活动性由强到弱的顺序是___________________。
(3)金属腐蚀造成的损失巨大,对金属腐蚀的控制尤为重要。下列对金属的防护措施不合理的是_______填序号)。
a.齿轮表面涂油 b.将钢材深埋保存
c.将钢刀浸泡在盐水中 d.车圈镀铬
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤厂为减少SO2的排放,可采取的措施是:
①洗涤含SO2的烟气,下列物质可作洗涤剂的是 .
a.浓NH3H2O b.NaHCO3 c.FeCl3 d.NaHSO3
②将煤转化为清洁气体燃料,过程如图所示: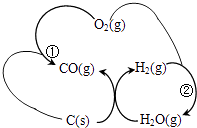
已知:反应①生成1molCO(g)的反应热△H=﹣110.5KJ/mol反应②生成1molH2O(g)的反应热△H=﹣241.6KJ/mol焦炭与水蒸气反应的热化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐是日常生活的必需品,也是重要的化工原料。粗食盐常含有少量Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaC1的流程如下:
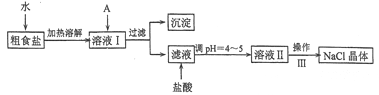
(1)加入A试剂,是为了除去溶液I中的Ca2+、Mg2+、Fe3+、SO42-离子。A代表的是多种试剂,按滴加顺序依次为:iNaOH,ⅱ__________,ⅲ_________(填化学式)。
(2)请写出下列试剂加入试剂i时发生主要反应的离子反应方程式:_________
(3)右下图是某学生的过滤操作示意图,其操作不规范的是________(填标号)。
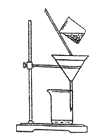
a.漏斗末端颈尖未紧靠烧杯壁
b.玻璃棒用作引流
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(4)操作III的名称是__________
(5)mg粗盐提纯后得到ng纯净的NaCl固体,则m与n的大小关系为_________.
A.m>n B. m=n C. m<n D. 无法确定.
(6)实验室需配制480 mL0.400mol/L盐酸,现用如图所示浓盐酸配制,回答下列问题:
盐酸
分子式: HCl
相对分子质量: 36.5
密度: 1.2g/cm3
HCl的质量分数为: 36.5%
①配制需要的玻璃仪器有玻璃棒、量简、烧杯、________(填仪器名称)
②需量取浓盐酸的体积为:__________mL。(结果保留1位小数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com