
【题目】NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,2.24 L水含有的分子数为0.1NA
B. 12g14C含有的中子数为8NA
C. 1 L0.1 mol·L-1 FeCl3溶液含阳离子数大于0.1NA
D. 1molN2和3 mol H2充分反应后,生成气体的分子数为2NA
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:
【题目】1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4 ℃,熔点9.79 ℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可以用下图所示装置制备1,2-二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。
填写下列空白:

(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式: 。
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象: 。
(3)容器c中NaOH溶液的作用是: 。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多。如果装置的气密性没有问题,试分析其可能的原因: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25 ℃时,某浓度NaCN(氰化钠)溶液pH=11,则下列有关说法中不正确的是( )
A. HCN的电离方程式:HCN![]() H++CN-
H++CN-
B. NaCN是一种弱电解质
C. NaCN溶液中一定存在:c(Na+)>c(CN-)
D. 0.1 mol·L-1NaCN溶液中:c(CN-)+c(HCN)=0.1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,只有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图所示。

(1)基态硼原子的电子排布式为___________________。
(2)下列关于这两种晶体的说法,正确的是______________(填序号)
a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体的B-N键均为共价键
d.两种晶体均为分子晶体
e.立方相氮化硼的晶体晶胞中,含有4个B原子,4个N原子
(3)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为___________,其结构与石墨相似却不导电,原因是________________________________。
(4)立方氮化硼和金刚石是等电子体,其晶胞如图所示,则处于晶胞顶点上的原子配位数为________________,若晶胞边长为361.5pm,则立方氮化硼的密度是______________g·cm-3(只要求列算式,不必计算出数值,阿伏加德罗常数的值为NA)。

(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一,1mol NH4BF4含有___________mol配位键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将SO2通入略显酸性的Fe(NO3)3溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时若滴入BaCl2溶液,则会产生白色沉淀,在上述一系列变化过程中,最终被还原的微粒是
A.NO3-B.SO2C.Fe2+D.Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法中,正确的一组是
① 和
和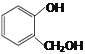 互为同系物
互为同系物
②蛋白质水解和油脂皂化都是高分子生成小分子的过程
③高分子材料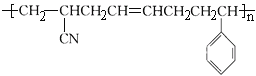 是由三种单体聚合而成的,该高分子材料是体型结构高分子,具有热固性
是由三种单体聚合而成的,该高分子材料是体型结构高分子,具有热固性
④C2H2 和C6H6不论二者以何种比例混合,只要总质量一定,则完全燃烧时消耗O2和生成的H2O的质量不变
⑤塑料、合成橡胶和合成纤维都是合成高分子材料
⑥棉花、蚕丝、人造丝的主要成分都是纤维素
A. ②③④⑤ B. ①③⑤ C. ④⑤ D. ①③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用吸附了氢气的纳米碳管等材料制作的二次电池的原理如右图。下列说法正确的是

A. 放电时,负极发生还原反应
B. 放电时,正极的电极反应为:NiO(OH)+H2O+e-=Ni(OH)2+OH-
C. 放电时,OH-移向镍电极
D. 充电时,将电池的镍电极与外电源的负极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 离子化合物中只能含有离子键
B. 共价化合物中可能含有离子键
C. 化学键存在于分子之间
D. 化学反应的过程,本质上是旧化学键断裂和新化学键形成的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某研究性学习小组设计的对一种废旧合金的各成分(含有Cu、Fe、Si 三种成分)进行分离、回收再利用的工业流程,通过该流程将各成分转化为常用的单质及化合物。

已知:298K时,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=4.0×10-38, Ksp[Mn(OH)2] =1.9×10-13,
根据上面流程回答有关问题:
(1)操作Ⅰ、Ⅱ、Ⅲ指的是 。
(2)加入过量FeCl3溶液过程中可能涉及的化学方程式: 。
(3)过量的还原剂应是 。
(4)①向溶液b中加入酸性KMnO4溶液发生反应的离子方程式为 。
②若用X mol/L KMnO4溶液处理溶液b,当恰好将溶液中的阳离子完全氧化时消耗KMnO4溶液YmL,则最后所得红棕色固体C的质量为 g(用含X、Y的代数式表示)。
(5)常温下,若溶液c中所含的金属阳离子浓度相等,向溶液c中逐滴加入KOH溶液,则三种金属阳离子沉淀的先后顺序为: ﹥ ﹥ 。(填金属阳离子)
(6)最后一步电解若用惰性电极电解一段时间后,析出固体B的质量为Z g,同时测得阴阳两极收集到的气体体积相等,则标况下阳极生成的最后一种气体体积为 L(用含Z的代数式表示);该电极的反应式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com