【答案】
分析:1.X为无色液体,推断X为H
2O;
2.D具有两性,可知D为Al
2O
3或Al(OH)
3,而Al
2O
3要经过氢氧化铝脱水或铝直接与氧气化合而得,图中显然不具备这样的条件,因此D为Al(OH)
3,D由A反应而来,A中含铝元素;
3.因为D遇I溶解,可知I为强酸或强碱,但I由J一路反应而来,又有J为第二周期元素的气态氢化物,因此J为非金属氢化物,I为强酸,而L+X生成I+K,只有硝酸的生成(3NO
2+H
2O=2HNO
3+NO)符合这一模式,I为HNO
3;L为NO
2,K为NO,由NO+F到NO
2,F为O
2.顺便也可知J中含氮元素,J为NH
3;
4.因为C也为第二周期元素的气态氢化物,而第二周期元素的气态氢化物一般只研究碳与氮元素的氢化物(若C为HF,则A为AlF
3,不合题意;而硼的性质一般不做研究,否则要给提示或条件),J为NH
3,所以C为烃类,A为碳与铝的化合物,结合给出的质量分数,A为Al
4C
3,它与水发生水解反应时,碳元素的价态不变,因此产物C为甲烷(CH
4),它与F(氧气)反应除水之外的产物H为CO
2.A+X=C+D反应方程式:Al
4C
3+12H
2O→4Al(OH)
3+3CH
4↑;
5.因为H与G反应生成D(Al(OH)
3),G由D反应来,因此G为偏铝酸盐,E为强碱,因为E由短周期元素化合物B与水反应来,所以E为NaOH,G为NaAlO
2,因为B+水生成NaOH+O
2,所以B为Na
2O
2.依据推断物质分析回答问题.
解答:解:1.X为无色液体,推断X为H
2O;
2.D具有两性,可知D为Al
2O
3或Al(OH)
3,而Al
2O
3要经过氢氧化铝脱水或铝直接与氧气化合而得,图中显然不具备这样的条件,因此D为Al(OH)
3,D由A反应而来,A中含铝元素;
3.因为D遇I溶解,可知I为强酸或强碱,但I由J一路反应而来,又有J为第二周期元素的气态氢化物,因此J为非金属氢化物,I为强酸,而L+X生成I+K,只有硝酸的生成(3NO
2+H
2O=2HNO
3+NO)符合这一模式,L为NO
2,K为NO,由NO+F到NO
2,F为O
2.顺便也可知J中含氮元素,J为NH
3;
4.因为C也为第二周期元素的气态氢化物,而第二周期元素的气态氢化物一般只研究碳与氮元素的氢化物(若C为HF,则A为AlF
3,不合题意;而硼的性质一般不做研究,否则要给提示或条件),J为NH
3,所以C为烃类,A为碳与铝的化合物,结合给出的质量分数,A为Al
4C
3,它与水发生水解反应时,碳元素的价态不变,因此产物C为甲烷(CH
4),它与F(氧气)反应除水之外的产物H为CO
2.A+X=C+D反应方程式:Al
4C
3+12H
2O→4Al(OH)
3+3CH
4↑;
5.因为H与G反应生成D(Al(OH)
3),G由D反应来,因此G为偏铝酸盐,E为强碱,因为E由短周期元素化合物B与水反应来,所以E为NaOH,G为NaAlO
2,因为B+水生成NaOH+O
2,所以B为Na
2O
2.综上所述判断出的各物质为:A为Al
4C
3 ;B为Na
2O
2;C为CH
4;D为Al(OH)
3;E为NaOH;F为O
2;G为NaAlO
2;H为CO
2;I为HNO
3;为NH
3;K为NO;LNO
2;X为H
2O;
(1)依据分析推断得到A、B、C分别为:Al
4C
3、Na
2O
2、CH
4,故答案为:Al
4C
3;Na
2O
2;CH
4;
(2)反应③为2Na
2O
2+2H
2O=4NaOH+O
2;反应中过氧化钠自身氧化还原反应,氧元素化合价从-1价变化为0价,-2价,反应中每生成lmolF(O
2)转移电子物质的量为2mol,转移电子数为1.204×10
24,故答案为:1.204×10
24;
(3)反应④是氨气的催化氧化反应,反应的化学方程式为:4NH
3+5O
2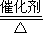
4NO+6H
2O,故答案为:4NH
3+5O
2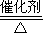
4NO+6H
2O;
(4)反应②是二氧化碳气体通入偏铝酸钠溶液中发生的反应,反应的离子方程式为:2AlO
2-+CO
2+3H
2O=2Al(OH)
3↓+CO
32-或AlO
2-+CO
2+2H
2O=2Al(OH)
3↓+HCO
3-;反应⑤是氢氧化铝在硝酸中溶解的反应,反应的离子方程式为:Al(OH)
3+3H
+=Al
3++3H
2O,
故答案为:2AlO
2-+CO
2+3H
2O=2Al(OH)
3↓+CO
32-或AlO
2-+CO
2+2H
2O=2Al(OH)
3↓+HCO
3-;Al(OH)
3+3H
+=Al
3++3H
2O;
(5)反应①是甲烷燃烧生成二氧化碳和水的反应,每1.00g CH
4与足量的F(O
2)作用,恢复到25℃水为液体,放出55.6kJ热量;依据化学方程式计算1mol甲烷燃烧放热为889.6KJ;
反应的热化学方程式为:CH
4(g)+2O
2(g)
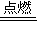
CO
2(g)+2H
2O(l)△H=-889.6kJ?mol
-1,
故答案为:CH
4(g)+2O
2(g)
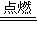
CO
2(g)+2H
2O(l)△H=-889.6kJ?mol
-1.
点评:本题考查了物质转化关系的分析判断,物质性质的应用,反应现象的分析,化学方程式、离子方程式、热化学方程式的书写方法和计算应用,物质性质的分析,现象的推断是解题关键.题目难度中等.


 4NO+6H2O,故答案为:4NH3+5O2
4NO+6H2O,故答案为:4NH3+5O2 4NO+6H2O;
4NO+6H2O;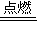 CO2(g)+2H2O(l)△H=-889.6kJ?mol-1,
CO2(g)+2H2O(l)△H=-889.6kJ?mol-1,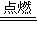 CO2(g)+2H2O(l)△H=-889.6kJ?mol-1.
CO2(g)+2H2O(l)△H=-889.6kJ?mol-1.






