
焦亚硫酸钠(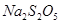 )常用作食品漂白剂,其制备工艺流程如下:
)常用作食品漂白剂,其制备工艺流程如下: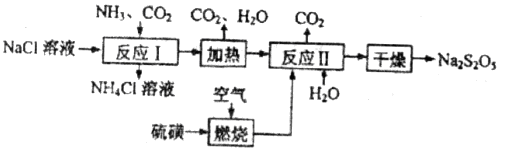
已知:反应Ⅱ包含 等多步反应。
等多步反应。
(1)反应Ⅰ的化学方程式为____________,反应Ⅰ进行时应先通入__________气体。
(2)硫磺燃烧前先加热成液态并通过喷嘴喷入焚硫炉中,目的是__________。在上述工艺流程中可循环使用的物质是_____________。
(3)反应Ⅱ中需控制参加反应的气体与固体的物质的量之比接近____________,若气体量不足,则会导致_______________。
(4)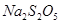 与稀硫酸反应放出
与稀硫酸反应放出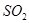 ,其离子方程式为___________。
,其离子方程式为___________。
(1)CO2+NH3+NaCl+H2O=NaHCO3↓+NH4Cl,NH3(1分)
(2)增大硫与空气的接触面积,使硫磺充分燃烧,加快反应速率,CO2和H2O
(3)2:1(1分),Na2S2O5产品中Na2SO3、Na2CO3等杂质含量增加,Na2S2O5产率降低。
(4)S2O52—+2H+=2SO2↑+H2O。
解析试题分析:(1)本题考查侯德榜制碱法的原理,利用碳酸氢钠的溶解度较小,反应方程式为CO2+NH3+NaCl+H2O=NaHCO3↓+NH4Cl,二氧化碳在水中的溶解度不大,氨气极易溶于水,为提高溶液中碳酸氢根的浓度,应先通入氨气;(2)硫磺燃烧前先加热成液态并通过喷嘴喷入焚硫炉中,目的是增大硫与空气的接触面积,使硫磺充分燃烧,加快反应速率;由流程图知,可循环利用的物质是CO2和H2O;(3)反应Ⅱ中涉及的反应为Na2CO3+2SO2+H2O=2NaHSO3,2NaHSO3 Na2S2O5+H2O,参加反应的气体与固体的物质的量之比接近2:1,若气体量不足,则会导致Na2S2O5产品中Na2SO3、Na2CO3等杂质含量增加,Na2S2O5产率降低。(4)Na2S2O5与稀硫酸反应放出SO2,其离子方程式为S2O52—+2H+=2SO2↑+H2O。
Na2S2O5+H2O,参加反应的气体与固体的物质的量之比接近2:1,若气体量不足,则会导致Na2S2O5产品中Na2SO3、Na2CO3等杂质含量增加,Na2S2O5产率降低。(4)Na2S2O5与稀硫酸反应放出SO2,其离子方程式为S2O52—+2H+=2SO2↑+H2O。
考点:考查化学工艺流程及化学方程式书写。


 百年学典课时学练测系列答案
百年学典课时学练测系列答案科目:高中化学 来源: 题型:填空题
据科学家预测:再过100年后,全球气温估计将上升大约1.4~5.8 ℃。根据这一预测,全球气温上升将给全球环境带来不可估测的影响,其中水资源的匮乏将是首当其冲。海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既能解决淡水资源缺乏的问题,又能充分利用海洋资源。
(1)就目前技术而言,结合能源消耗等问题,下列适用于“海水淡化”的技术是 (填序号)。
| A.蒸馏法; | B.电渗析法; | C.冷结法; | D.离子交换法;E.反渗透法 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(12分)【化学——化学与技术】
资源开发、材料制备及工农业生产等都离不开化学。请回答下列问题:
(1)工业制肥皂时,在皂化反应结束后需要在混合物中加入饱和食盐水。加入饱和食盐水的目的是 。
(2)Al2O3的熔点高达2050oC,工业上为了降低能量消耗,在金属铝的冶炼中通常采取的措施是 。
(3)工业上合成氨所需的氮气来源于 ,氢气来源于 ,写出工业上在催化剂作用下制取氢气的其中一个化学方程式 。
(4)工业制硫酸时,SO3的生成是在 (填设备名称)中进行的,工业上常采用浓硫酸吸收SO3,而不直接用水吸收的原因是 。在吸收塔中,为提高SO3的吸收率所采取的措施为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”(侯氏制碱法)两种工艺。
①“氨碱法”产生大量CaCl2废弃物,写出该工艺中产生CaCl2的化学方程式:_________________________________________________;
②写出“联合制碱法”有关反应的化学方程式_________________ _; 。
③CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同?________________________________________;
(2)钢铁工业对促进经济和社会发展起了重要作用。
①炼钢时,加入硅、锰和铝的目的是_______________________________。
②不锈钢含有的Cr元素是在炼钢过程的氧吹__ __(填“前”或“后”)加入。
③炼铁和炼钢生产中,尾气均含有的主要污染物是________。从环保和经济角度考虑,上述尾气经处理可用作_________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
工业上利用硫酸渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)制备高档颜料铁红(Fe2O3 )和回收(NH4)2SO4,具体生产流程如下:
回答下列问题:
(1)在废渣溶解操作时,为了加速废渣溶解的措施是:___________________、__________________(任写两点)
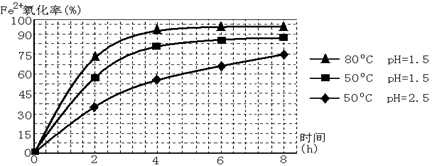
(2)物质A是一种氧化剂
①工业上最好选用 (填序号)
| A.空气 | B.Cl2 | C.MnO2 | D.H2O2, |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
工业上用白云石制备高纯氧化镁的工艺流程如下:
已知白云石的主要成分可表示为:
CaO 32.50%;MgO 20.58%;Fe2O3 2.18%;SiO2 0.96%;其他 43.78%
(1)为了提高白云石的煅烧效果,可以采取的措施是 。
若在实验室中煅烧白云石,需要的仪器除酒精灯、三脚架以外,还需要 。
| A.蒸发皿 | B.坩埚 | C.泥三角 | D.石棉网 |


查看答案和解析>>
科目:高中化学 来源: 题型:填空题
[化学-选修化学与技术](15分)
七水硫酸镁(MgSO4·7H2O)在印染、造纸和医药等工业上都有广泛的应用,利用化工厂生产硼砂的废渣-硼镁泥可制取七水硫酸镁。硼镁泥的主要成分是MgCO3,还含有其他杂质(MgO、SiO2、Fe2O3、FeO、CaO、Al2O3、MnO等)。
表1 部分阳离子以氢氧化物形式完全沉淀时溶液的pH
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
| pH值 | 5.2 | 3.2 | 9.7 | 10.4 | 11.2 |
| 温度/℃ | 10 | 30 | 40 | 50 | 60 |
| CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 | 0.19 |
| MgSO4·7H2O | 30.9 | 35.5 | 40.8 | 45.6 | / |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氮化硅( Si3N4)是一种优良的高温结构陶瓷,在工业生产和科技领域有重要用途.
I.工业上有多种方法来制备氮化硅,常见的方法有:
方法一:直接氮化法:在1300℃-1400℃时,高纯粉状硅与纯氮气化合,其反应方程式为
。
方法二:化学气相沉积法:在高温条件下利用四氯化硅气体、纯氮气、氢气反应生成氮化硅和HC1,与方法一相比,用此法制得的氮化硅纯度较高,其原因是 .
方法三:Si(NH2)4热分解法:先用四氯化硅与氨气反应生成Si(NH2)4和一种气体(填分子式)________;然后使Si(NH2)4受热分解,分解后的另一种产物的分子式为 。
II.工业上制取高纯硅和四氯化硅的生产流程如下:
已知:X、高纯硅、原料B的主要成分都可与Z反应,Y与X在光照或点燃条件下可反应,Z的焰色呈黄色.
(1)原料B的主要成分是(写名称) 。
(2)写出焦炭与原料B中的主要成分反应的化学方程式: 。
(3)上述生产流程中电解A的水溶液时,阳极材料能否用Cu (填“能”或“不能”),写出Cu为阳极电解A的水溶液开始一段时间阴阳极的电极方程式:
阳极: ;阴极: 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
化学工业在经济发展中的作用举足轻重。下列有关工业生产的叙述中,正确的是 ( )
| A.硫酸生产中常采用高压条件来提高SO2的转化率 |
| B.合成氨中采用及时分离液态氨来提高反应速率 |
| C.电解精炼铜中,溶液中c(Cu2+)基本保持不变 |
| D.氯碱工业中阳极得到氢氧化钠和氢气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com