
同周期的A、B、C三元素,其最高价氧化物对应水化物的酸性强弱顺序是HAO4>H2BO4>H3CO4,则下列判断错误的是
A.非金属性A>B>C
B.气态氢化物稳定性HA>H2B>CH3
C.原子半径A>B>C
D.阴离子还原性C3->B2->A-
科目:高中化学 来源:2014高考名师推荐化学化学平衡图像(解析版) 题型:实验题
某校学生化学实验小组,为验证非金属元素氟的氧化性强于硫和氮,设计了一套实验装置:(部分加持装置已略去)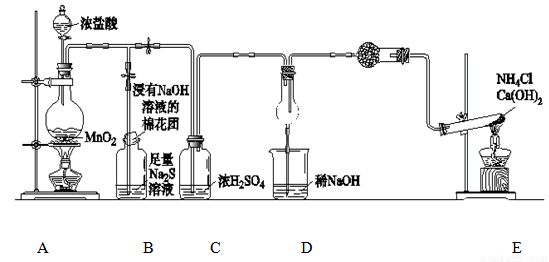
(1)写出A中反应的离子方程式 。
(2)B中出现黄色浑浊现象,产生此现象的离子方程式 。
(3)试从原子结构角度解释氯的氧化性大于硫的原因 。
(4)D中干燥管中出现的现象及化学方程式 。
(5)有同学认为D中的现象并不能说明氯的氧化性大于氮,需要在C之前加装洗气装置,请画出其装置图 (并注明盛装试剂)。
(6)还有什么方法能证明氧化性Cl2>S,用一种相关事实说明 。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学制备实验方案的设计与评价(解析版) 题型:实验题
如图所示是一套实验室制气装置,用于发生、干燥和收集气体。下列各组物质中能利用这套装置进行实验的是
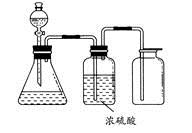
A.铜屑和稀硝酸
B.二氧化锰和浓盐酸
C.用浓氨水和生石灰反应
D.碳酸钙和稀盐酸
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学元素周期律及化学键(解析版) 题型:选择题
已知33As、35Br位于同一周期,下列关系正确的是
A 原子半径:As>C1>P B 热稳定性:HC1>AsH3>HBr
C 还原性:As3->S2->C1- D 酸性:H3AsO4>H2SO4>H3PO4
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学元素周期律及化学键(解析版) 题型:选择题
短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁原子最外层电子数与电子层数相等,则
A、原子半径:丙>丁>乙
B、单质的还原性:丁>丙>甲
C、甲、乙、丙的氧化物均为共价化合物
D、乙、丙、丁的最高价氧化物对应的水化物不能相互反应
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学元素周期律及其应用(解析版) 题型:选择题
下列说法正确的是
A.第ⅥA族元素从上到下,其氢化物的稳定性逐渐减弱
B.L层电子数为奇数的所有元素都是非金属元素
C.ⅦA族元素阴离子的还原性越强,元素的最高价氧化物对应水化物的酸性也越强
D.同一主族的甲乙两种元素,甲的原子序数为a,则乙的原子序数可能为a+4
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学乙醇和乙酸(解析版) 题型:选择题
某有机物的化学式为C4H8O3,现有0.1 mol该有机物分别与足量的钠、足量的碳酸氢钠溶液反应,生成标准状况下的气体分别为2.24 L H2、2.24 L CO2。则该有机物的同分异构体有(不考虑立体异构)
A.3种 B.4种C.5种D.6种
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学Vm与它的推论应用(解析版) 题型:选择题
在体积相同的两个密闭容器中分别充满O2、O3气体,当这两个容器内温度、密度相等时,下列说法正确的是
A.两种气体的压强相等
B.O2比O3质量小
C.两种气体的分子数目相等
D.两种气体的氧原子数目相等
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学CB计算法(解析版) 题型:选择题
用NA表示阿伏加德罗常数,下列结论能够成立的是
A.0.1 mol·L-1的Na2CO3溶液中含有CO32-的个数是小于0.1NA
B.1 molFe与足量稀硝酸完全反应转移的电子数为2NA
C.0.2mol·L-1 CuSO4溶液加水稀释至体积增加1倍,其浓度变为0.1 mol·L-1
D.4g NaOH固体溶解1L水中,所得溶液的物质的量浓度为0.1mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com