
(18分)(1)一定温度下,向1 L 0.1 mol·L-1 CH3COOH溶液中加入0.1 mol CH3COONa固体,则醋酸的电离平衡向________(填“正”或“逆”)向移动;溶液中 的值________(填“增大”、“减小”或“不变”)。
的值________(填“增大”、“减小”或“不变”)。
(2)氨气的水溶液称为氨水,其中存在的主要溶质微粒是NH3·H2O。
已知:a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5;
b.CH3COOH+NaHCO3 CH3COONa+CO2↑+H2O。
CH3COONa+CO2↑+H2O。
则CH3COONH4溶液呈________性(填“酸”、“碱”或“中”,下同),NH4HCO3溶液呈________性,NH4HCO3溶液中物质的量浓度最大的离子是________(填化学式)。
(3)99 ℃时,Kw=1.0×10-12,该温度下测得0.1 mol·L-1Na2A溶液的pH=6。
①H2A在水溶液中的电离方程式为_____________________________。
②该温度下,将0.01 mol·L-1 H2A溶液稀释到20倍后,溶液的pH=________。
③体积相等、pH=1的盐酸与H2A溶液分别与足量的Zn反应,产生的氢气_____。
A.盐酸多 B.H2A多 C.一样多 D.无法确定
④将0.1 mol·L-1 H2A溶液与0.2 mol·L-1氨水等体积混合,完全反应后溶液中各离子浓度从大到小的顺序为_______________________________________。
(1)逆 不变
(2)中 碱 NH4+
(3)①H2A 2H++A2- ② 3 ③ C ④c(NH4+)>c(A2-)>c(H+)>c(OH-)
2H++A2- ② 3 ③ C ④c(NH4+)>c(A2-)>c(H+)>c(OH-)
【解析】
试题分析:(1)一定温度下,向1 L 0.1 mol·L-1 CH3COOH溶液中加入0.1 mol CH3COONa固体,因为醋酸溶液中存在CH3COOH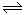 H++CH3COO-,则醋酸根离子浓度增大,平衡逆向移动;
H++CH3COO-,则醋酸根离子浓度增大,平衡逆向移动;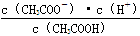 即为醋酸的电离常数,因为温度不变,所以电离常数不变;
即为醋酸的电离常数,因为温度不变,所以电离常数不变;
(2)醋酸与NH3·H2O的电离平衡常数相同,则铵根离子与醋酸根离子的水解程度相同,所以溶液呈中性;醋酸的酸性比碳酸强,所以碳酸氢根离子的水解程度大于醋酸根离子的水解程度也大于铵根离子的水解程度,碳酸氢根离子的水解使溶液呈碱性,所以碳酸氢铵溶液呈碱性;则NH4HCO3溶液中物质的量浓度最大的离子是NH4+;
(3)①99 ℃时,Kw=1.0×10-12,c(H+)=c(OH-)=10-6mol/L,因此pH=6的溶液为中性。则该温度下测得0.1 mol·L-1 Na2A溶液的pH=6,所以H2A为二元强酸,完全电离,电离方程式为H2A 2H++A2-;
2H++A2-;
②该温度下,0.01 mol·L-1 H2A溶液中氢离子的物质的量浓度是0.02mol/L,稀释到20倍后,氢离子浓度变为0.02mol/L/20=0.001mol/L,溶液的pH=-lg0.001=3;
③体积相等、pH=1的盐酸与H2A溶液中氢离子的物质的量相等,则与足量的Zn反应时产生的氢气一样多,答案选C;
④将0.1 mol·L-1 H2A溶液与0.2 mol·L-1氨水等体积混合,二者恰好完全反应生成(NH4)2A和水,铵根离子水解使溶液呈酸性,所以溶液中离子浓度的大小关系是c(NH4+)>c(A2-)>c(H+)>c(OH-)。
考点:考查电解质的电离平衡移动的判断,电离常数的判断,离子浓度的比较,电解质强弱的判断,盐的水解程度的比较,溶液酸碱性的判断


科目:高中化学 来源:2014-2015学年四川省高一12月月考化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.在水溶液中: H+、I―、NO3―、SiO32-
B.水溶液中:Cl-、NO3-、Na+、SO32-
C.将足量CO2通入时:H+、NH4+、AlO2-、SO42-
D.碱性溶液中:NO3-、I-、Na+、Al3+
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省枣庄市高三1月月考理综化学试卷(解析版) 题型:填空题
(20分)氮氧化物(NOx)、SO2和CO2等气体会造成环境问题。对燃煤废气进行脱硝、 脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g) + 4NO2(g) =4NO(g) + CO2(g) + 2H2O(g) △H1=-574 kJ·mol-1
CH4(g) + 4NO(g) =2N2(g) + CO2(g) + 2H2O(g) △H2=-1160 kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为 。
(2)脱碳。将CO2转化为甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2进行上述反应。测得CO2和CH3OH(g)浓度随时间变化如图所示。

则0~10 min内,氢气的平均反应速率为 _______mol/(L·min);第10 min后,保持温度不变,向该密闭容器中再充入1 mol CO2(g)和1 mol H2O(g),则平衡 (填“正向”、“逆向”或“不”)移动。
(3)脱硫。利用Na2SO3溶液可脱除烟气中的SO2。Na2SO3可由NaOH溶液吸收SO2制得。NaOH溶液吸收SO2的过程中,pH随n(SO32-)︰n(HSO3﹣)变化关系如下表:
n(SO32﹣)︰n(HSO3﹣) | 91︰9 | 1︰1 | 9︰91 |
pH | 8.2 | 7.2 | 6.2 |
①由上表判断,NaHSO3溶液显 性,用化学平衡原理解释: 。
②当溶液呈中性时,离子浓度关系正确的是(选填字母): 。
a.c(Na+)=2c(SO32-)+c(HSO3-)
b.c(Na+) > c(HSO3-) > c(SO32-) > c(H+) = c(OH-)
c.c(Na+) + c(H+) = c(SO32-) + c(HSO3-) + c(OH-)
(4)利用下图所示装置(电极均为惰性电极)可吸收SO2,用阴极排出的溶液可吸收NO2。

①阳极的电极反应式为_________________。
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有 生成。该反应中氧化剂与还原剂的物质的量之比为_______________。
生成。该反应中氧化剂与还原剂的物质的量之比为_______________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期12月月考化学试卷(解析版) 题型:选择题
下列化学事实的描述或解释正确的是
A.Na2SO3溶液中:c(H+)+c(HSO3-)+2c(H2SO3)===c(OH-)
B.NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-==CO32-+H2O
C.有些化学反应既属于复分解反应又属于氧化还原反应
D.常温下,将pH=3的HA和PH=11的BOH等体积混合后PH>7,可能生成了弱酸强碱盐
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期12月月考化学试卷(解析版) 题型:选择题
下列有关结构和性质的说法正确的是
A.元素铯的两种核素137Cs比133Cs多4个质子
B.元素P、S、Cl得电子能力和最高价氧化物对应水化物的酸性均依次增强
C.元素原子的最外层电子数越多,越容易得电子
D.比黄金还贵的18O2和普通的16O2是两种不同的核素
查看答案和解析>>
科目:高中化学 来源:2014-2015学年内蒙古巴彦淖尔市高三上学期期中考试化学试卷(解析版) 题型:选择题
将浓度为0.1 mol·L-1 HF溶液加水不断稀释,下列各量始终保持增大的是
A.c(H+) B.Ka(HF) C.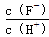 D.
D.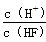
查看答案和解析>>
科目:高中化学 来源:2014-2015学年内蒙古巴彦淖尔市高三上学期期中考试化学试卷(解析版) 题型:选择题
在密闭容器中进行如下反应:X2(气) + Y2(气)  2Z(气), 已知 X2、Y2、Z的起始浓度分别为 0.1 mol/L, 0.3 mol/L, 0.2 mol/L, 在一定的条件下, 当反应达到平衡时, 各物质的浓度不可能的是
2Z(气), 已知 X2、Y2、Z的起始浓度分别为 0.1 mol/L, 0.3 mol/L, 0.2 mol/L, 在一定的条件下, 当反应达到平衡时, 各物质的浓度不可能的是
A.Z 为 0.3 mol/L B.Y2 为 0.35 mol/L
C.X2 为 0.12 mol/L D.Z 为 0.4 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 步骤 | 操作 | 现象 |
| ① | 用pH试纸检验 | 溶液的pH大于7 |
| ② | 向溶液中滴加氯水,再加入CCl4、振荡、静置 | CCl4层呈橙色 |
| ③ | 取②的上层溶液,加入Ba(NO3)2溶液和稀HNO3 | 有白色沉淀产生 |
| ④ | 将③过滤,向滤液中加入AgNO3溶液和稀HNO3 | 有白色沉淀产生 |
| A、肯定含有的离子是①④⑤ |
| B、肯定没有的离子是②⑤⑦ |
| C、可能含有的离子是①②⑥ |
| D、不能确定的离子是①③⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com