
【题目】KClO3和浓盐酸在一定温度下发生如(1)的反应:
(1)请配平方程式,并用双线桥表示得失电子情况:
_____KClO3+______HCl(浓)=______KCl+______ClO2↑+______Cl2↑+______H2O
(2)氧化剂是_________,还原产物是_________(写化学式)。
(3)产生0.1molCl2时,转移电子的物质的量为__________mol。
【答案】(1)
(2)KClO3 ClO2 (3)(1分)0.2
【解析】
试题分析:(1)KClO3中氯元素化合价由+5价降低为ClO2中+4价,化合价降低1价;HCl中氯元素化合价由-1价升高为Cl2中0价,化合价升高2价,化合价升降最小公倍数为2,故ClO2系数为2,Cl2系数为1;所以KClO3系数为2,KCl系数为2,HCl系数为4,结合原子守恒配平方程式,其反应方程式为:
2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O,用双线桥分析电子的得失情况是: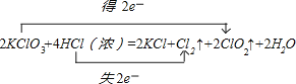 ;
;
(2)此反应中氯酸钾中氯元素的化合价从+5价降为+4价,可知氧化剂是KClO3,对应的还原产物是ClO2;
(3)该反应中氯气和转移电子的关系为1:2,则产生0.1mol Cl2,则转移的电子的物质的量为0.2mol。


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.活化分子间的碰撞一定发生化学反应
B.吸热反应只有加热才能发生
C.有能量变化的一定是化学反应
D.有化学键断裂不一定发生化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应2A(s)+3B(g)![]() C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
①增加A的量,平衡向正反应方向移动
②升高温度,反应速率增大,平衡向逆反应方向移动
③压缩容器增大压强,平衡不移动,v(正)、v(逆)不变
④增大B的浓度,v(正)>v(逆)
⑤加入催化剂,B的转化率提高
A.①② B.② C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5。已知:① 装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2===Na2S2O5;
② Na2S2O5晶体在空气中被氧化生成Na2SO4。
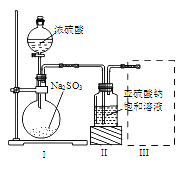
(1) 装置Ⅰ中产生气体的化学方程式为:_____________________________。
(2) 要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是 。
(3) 装置Ⅲ用于处理尾气,可选用右图中最合理装置(夹持仪器已略去)为___________(填序号)。
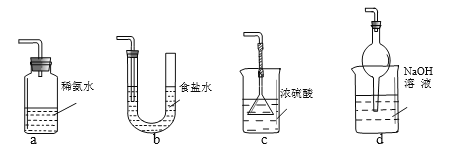
(4)检测Na2S2O5晶体在空气中已被氧化的实验方案是: 。
(5)为了研究Cl2与SO2的在干燥条件下发生反应及进行的程度。用右下图所示装置收集满干燥的Cl2,再通入干燥的SO2,集气瓶中立即出现无色液体SO2Cl2; 充分反应后,将液体和剩余气体分离。用除尽空气的NaOH溶液吸收分离出的气体,用足量稀盐酸酸化后,再滴加BaCl2溶液,产生白色沉淀,该白色沉淀是 ,由此可知反应后剩余的气体为Cl2和 ,综合实验信息,干燥的SO2与Cl2反应的化学方程式为 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等量的苛性钠溶液分别用pH值为2和3的醋酸溶液中和,设消耗醋酸溶液的体积依次为Va和Vb,则它们之间的关系是
A. Va>10Vb B. Vb=10Va C. Va<10Vb D. Vb>10Va
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法,错误的是( )
A. 乙酸乙酯在一定条件下可以水解成乙醇和乙酸
B. 油脂和蔗糖都属于高分子化合物
C. 油脂水解能得到甘油
D. 淀粉、纤维素在一定条件下水解均可得到葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列水溶液中的各组离子因为发生氧化还原反应而不能大量共存的是
A. Na+、Ba2+、Cl-、SO42-
B. Ca2+、HCO3-、C1-、K+
C. MnO4-、K+、I-、H+
D. H+、Cl-、Na+、CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com