D
分析:A、标准状况下,22.4L CO
2的物质的量为1mol;
B、计算溶质的物质的量,结合溶质的组成计算电离出Na
+的数目;
C、根据化合价和物质的量计算转移的电子数目;
D、根据溶质的物质的量,结合溶质的组成计算Cl
-数目.
解答:A、标准状况下,22.4L CO
2的物质的量为1mol,含有的分子数为N
A,故A正确;
B、10.6g Na
2CO
3的物质的量为
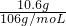
=0.1mol,则电离出Na
+的数目为0.2N
A,故B正确;
C、1mol CuO被还原成Cu,Cu的化合价由+2价降到0价,得到电子数目为2N
A,故C正确;
D、1L0.5mol/L的FeCl
3溶液中,含有Cl
-的物质的量为1L×0.5mol/L×3=1.5mol,Cl
-数目为1.5N
A,故D错误.
故选D.
点评:本题考查阿伏加德罗常数知识,题目难度不大,注意物质的组成、结构、状态、性质及存在条件等.

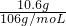 =0.1mol,则电离出Na+的数目为0.2NA,故B正确;
=0.1mol,则电离出Na+的数目为0.2NA,故B正确;

 高中必刷题系列答案
高中必刷题系列答案