
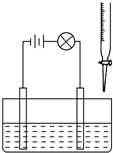
 在烧杯里加入20mL 0.1mol?L-1的Ba(OH)2溶液,再滴几滴酚酞试液,然后用滴定管向烧杯中滴加等物质的量浓度的NaHSO4溶液.实验装置如图(夹持仪器已去掉):
在烧杯里加入20mL 0.1mol?L-1的Ba(OH)2溶液,再滴几滴酚酞试液,然后用滴定管向烧杯中滴加等物质的量浓度的NaHSO4溶液.实验装置如图(夹持仪器已去掉):

科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
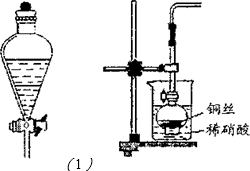
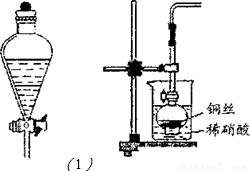
在化学实验中分液漏斗有诸多刚途,请按要求回答:
I、用分液漏斗进行分液,从所示的分液漏斗中将下层液体
放出的操作步骤为:
① ;
②旋开活塞,使下层液体流出到一个烧杯里,当下层液体
全部流出活塞的细孔时, ;
③从漏斗上口倒出上层液体;
④旋开活塞,将留在颈部的下层液体放出到盛接下层液体的
烧杯里。
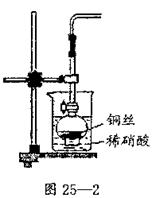
II、用烧杯、分液漏斗、导管和铁架台组装了一套制取NO气
体的简易发生装置,如图25—2所示。该气体发生装置的优点
是 。

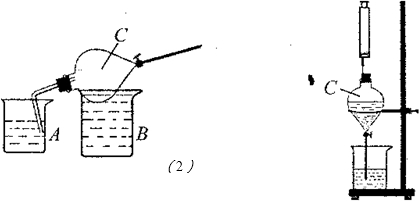
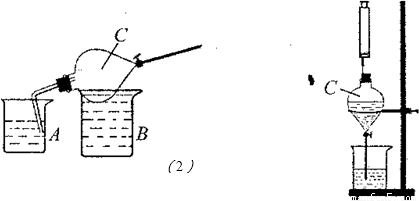
III、用下图所示装置来制取氨气,并完成喷泉实验操作步骤:

①如图25—3所示,向分液漏斗C加入约20mL的浓氨水,用连有直角导管的橡皮塞塞住上口;
②放在B装置中,用70℃的水浴加热一段时间;
③迅速将迮有直角导管的橡皮塞拔山,塞上插有注射器的橡皮塞(如图25—4),用注射器向分液漏斗中注入蒸馏水,打开旋塞,形成喷泉。
(1)为判断氨气已经收集满,需要A烧杯中盛放的试剂是 。
(2)图25—4中产生喷泉的原理是 。
查看答案和解析>>
科目:高中化学 来源:绍兴一中2009—2010学年第一学期高三期末调测化学试题 题型:实验题
(10分)在化学实验中分液漏斗有诸多刚途,请按要求回答:
I、用分液漏斗进行分液,从所示的分液漏斗中将下层液体
放出的操作步骤为:
① ;
②旋开活塞,使下层液体流出到一个烧杯里,当下层液体
全部流出活塞的细孔时, ;
③从漏斗上口倒出上层液体;
④旋开活塞,将留在颈部的下层液体放出到盛接下层液体的
烧杯里。
II、用烧杯、分液漏斗、导管和铁架台组装了一套制取NO气
体的简易发生装置,如图25—2所示。该气体发生装置的优点
是 。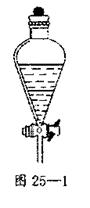
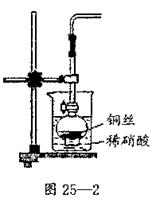
III、用下图所示装置来制取氨气,并完成喷泉实验操作步骤: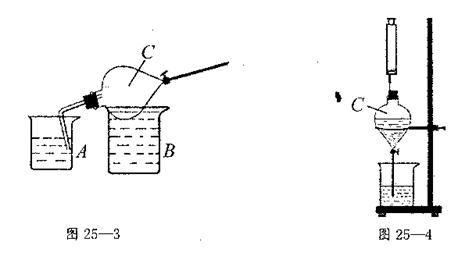
①如图25—3所示,向分液漏斗C加入约20mL的浓氨水,用连有直角导管的橡皮塞塞住上口;
②放在B装置中,用70℃的水浴加热一段时间;
③迅速将迮有直角导管的橡皮塞拔山,塞上插有注射器的橡皮塞(如图25—4),用注射器向分液漏斗中注入蒸馏水,打开旋塞,形成喷泉。
(1)为判断氨气已经收集满,需要A烧杯中盛放的试剂是 。
(2)图25—4中产生喷泉的原理是 。
查看答案和解析>>
科目:高中化学 来源:2009-2010学年浙江省绍兴一中高三(上)期末化学试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com