
某温度下,在一个2L的密闭容器中加入4mol A和2mol B进行如下反应:3A(g)+2B(g)⇌4C(s)+D(g),反应2min后达到平衡,测得生成1.6mol C,下列说法正确的是( )
|
| A. | 前2 min D的平均反应速率为0.2 mol•L﹣1•min﹣1 |
|
| B. | 此时,B的平衡转化率是40% |
|
| C. | 增大该体系的压强,平衡不移动 |
|
| D. | 增加B,平衡向右移动,B的平衡转化率增大 |
| 化学平衡的影响因素.. | |
| 专题: | 化学平衡专题. |
| 分析: | A.根据消耗的物质的量之比等于化学计量数之比计算生成的D的物质的量,根据v= B.根据方程式计算参加反应的B的物质的量,再根据转化率定义计算; C.该反应是气体的体积减小的反应,增大压强平衡向气体体积减小的反应; D.增大某一反应物的浓度,平衡向正反应移动,其它反应物的转化率增大,自身转化率降低. |
| 解答: | 解:A.反应2min后达到平衡,测得生成1.6molC,根据消耗的物质的量之比等于化学计量数之比,则生成0.4molD,v(D)= B.根据方程式可知,参加反应的B的物质的量=1.6mol×=0.8mol,故B的转化率= C.该反应是气体的体积减小的反应,增大压强平衡向气体体积减小的反应,故C错误; D.增加B的用量,B的浓度增大,平衡向正反应方向移动,A的转化率增大,但B的转化率降低,故D错误; 故选B. |
| 点评: | 本题考查化学平衡常数、化学反应速率与化学平衡计算、影响化学平衡的因素等,难度不大,注意掌握外界条件对化学平衡的影响. |


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
下列溶液Cl-物质的量浓度与50 mL 1 mol·L-1AlCl3溶液中Cl-物质的量浓度相等的是( )
A.150 mL 1 mol·L-1NaCl溶液 B.75 mL 1.5 mol·L-1CaCl2溶液
C.150 mL 3 mol·L-1KClO3溶液 D.50 mL 3 mol·L-1MgCl2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
设C+CO2==2CO(正反应吸热),该反应速率v1;N2+3H2  2NH3(正反应放热),该反应速率v2。若升温,v1和v2的变化是
2NH3(正反应放热),该反应速率v2。若升温,v1和v2的变化是
A.同时增大 B.同时减少
C.v1增大,v2减少 D.v1减少,v2增大
查看答案和解析>>
科目:高中化学 来源: 题型:
恒温、恒压下,在一个容积可变的容器中发生如下反应:
N2(g) + 3H2(g)  2NH3(g)
2NH3(g)
(1)若开始时放入1mol N2和3 molH2,达到平衡后,生成a mol NH3,这时N2的物质的量为 mol;
(2)若开始时无NH3,只放入N2和H2,达到平衡时生成NH3的物质的量为3a mol,则开始时放入N2和H2的物质的量分别为 mol和 mol;
(3)若开始时放入x mol N2、6 molH2和2 molNH3,达到平衡后,N2和NH3的物质的量分别为y mol和3a mol,则x= ,y= ,平衡时H2的物质的量_____(选填一个编号)。
A.大于6 mol B.等于6 mol C.小于6 mol D.可能大于、小于或等于6 mol
作出判断的理由是 ;
(4)若在(3)的平衡混合物中,再加入6 molNH3,再次达到平衡后,NH3的质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
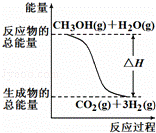
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJ/mol
②CH3OH(g)+O2(g)═CO2(g)+2H2(g)△H=﹣192.9kJ/mol
根据上述反应,下列说法正确的是( )
|
| A. | 反应①中的能量变化如图所示 |
|
| B. | CH3OH转变成H2的过程一定要吸收能量 |
|
| C. | 1mol CH3OH充分燃烧放出的热量为192.9kJ |
|
| D. | 可推知2H2(g)+O2(g)═2H2O(g)△H=﹣483.8 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
研究NO2、SO2、等大气污染气体的处理具有重要意义.
(1)NO2可用水吸收,相应的化学反应方程式为 3NO2+H2O=NO+2HNO3 .利用反应6NO2+8NH3 7N2+12H2O也可处理NO2.当转移1.2mol电子时,消耗的NO2在标准状况下是 6.72 L.
7N2+12H2O也可处理NO2.当转移1.2mol电子时,消耗的NO2在标准状况下是 6.72 L.
(2)已知:2SO2(g)+O2(g)⇌2SO3(g)△H=﹣196.6kJ•mol﹣1
2NO(g)+O2(g)⇌2NO2(g)△H=﹣113.0kJ•mol﹣1
则反应NO2(g)+SO2(g)⇌SO3(g)+NO(g)的△H= ﹣41.8 kJ•mol﹣1.
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 b .
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1mol SO3的同时生成1molNO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K= .
查看答案和解析>>
科目:高中化学 来源: 题型:
设计一个简单并能一次性完成的实验,验证醋酸、碳酸、苯酚的酸性强弱顺序是:CH3COOH>H2CO3>C6H5 OH
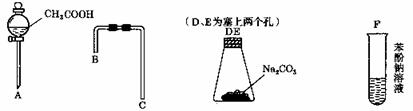
(1)仪器A的名称是 。
(2)利用上图所示的仪器可以组装实验装置,则仪器的连接顺序为: 接 ,
接 , 接 。
(3)有关反应的化学方程式为
。
(4)苯酚俗称 ,具有一定的杀菌能力,可以用作杀菌消毒剂,长期露置在空气中其表面会变为 色。
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值。下列判断正确的是 ( )
A.18gH2O含有的氢原子数目为NA
B.标准状况下,22.4LH2O含有的分子数目为NA
C.24g Mg变为Mg2+时失去的电子数为NA
D.常温常压下,71gCl2中含有的分子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com