


| ||
| 63.2g |
| 158g/mol |
 ��
�� ��
��| 63.2g |
| 158g/mol |


 �����Ծ�ϵ�д�
�����Ծ�ϵ�д� �ο�����������100��ϵ�д�
�ο�����������100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010��������һ�и�����ѧ�ڵ�һ���¿���ѧ�� ���ͣ������
KMnO4��Һ������������ԭ��Ӧ�ζ��ı�Һ������KMnO4��ǿ�����ԣ�������Һ�����ױ������л�ˮ��ijЩ�� ����ԭ�����ʻ�ԭ����������������MnO(OH)2���������KMnO4����Һ�IJ����ǣ�
����ԭ�����ʻ�ԭ����������������MnO(OH)2���������KMnO4����Һ�IJ����ǣ�
I.��ȡ�Զ�����������KMnO4��������ˮ������Һ���Ȳ�������1 h��
II. ���ײ���©����������ֽ�����˳�ȥ���ܵ�MnO(OH)2��
III. ���˵õ���KMnO4��Һ��������ɫ�Լ�ƿ���ڰ�����
IV. ����������ԭ�ζ���������700C��800C�������û��Լ������ȸߡ���Է��������ϴ��ȶ��ԽϺõ����ʣ�����ᾧ��H2C2O4?2H2O ����Һ�궨��Ũ�ȡ���֪�� MnO4-(H+)��Mn2+�� H2C2O4�� CO2��Ӧ������Ԫ��û�еá�ʧ���ӡ���ش��������⣺
��1��д���������ữ��������KMnO4��H2C2O4��Ӧ�����ӷ���ʽ�� ��
��2����α�֤��700C��800C�����½��еζ������� ��
��3��ȷ��ȡһ�������25.00 mL����KMnO4��Һʹ�õ������� ��
��4����ȷ��ȡW g���Լ�����ˮ���500 mLˮ��Һ��ȡ25.00 mL������ƿ�У��ø��������Һ�ζ����յ㣬���ĸ������ ��ҺV mL���ʣ�
��ҺV mL���ʣ�
�ٵζ��յ��־�� ��
��KMnO4��Һ�����ʵ���Ũ��Ϊ mol��L��1��
��5�����÷������ܵ�KMnO4����Һȥ�ζ�ˮ����Fe2����������õ�Ũ��ֵ�� -------���ƫ�ߡ���ƫ�͡���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ����ĩ�� ���ͣ�ʵ����
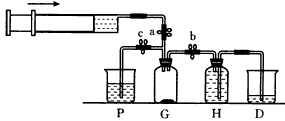
��֪��KMnO4+HCl(Ũ)��KCl+MnCl2+Cl2��+H2O��
�Իش��������⣺
(1)����ƽ������Ӧ��_____KMnO4+_____HCl(Ũ)=______KCl+_______MnCl2+______Cl2��+______H2O��
�ڵ���0.40 mol����ת��ʱ�����ɵ�Cl2�����Ϊ____L(��״����)��
(2)װ��H��ʢ�ŵ��Լ���________��
(3)β������ʱ���ɼ�_________���رյ��ɼ�a�͵��ɼ�________��
(4)����β��ʱ��������Ӧ�����ӷ���ʽΪ_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
KMnO4��Һ������������ԭ��Ӧ�ζ��ı�Һ������KMnO4��ǿ�����ԣ�������Һ�����ױ������л�ˮ��ijЩ������ԭ�����ʻ�ԭ����������������MnO(OH)2���������KMnO4����Һ�IJ����ǣ�
![]() I. ��ȡ�Զ�����������KMnO4��������ˮ������Һ���Ȳ�������1 h��
I. ��ȡ�Զ�����������KMnO4��������ˮ������Һ���Ȳ�������1 h��
![]() II. ���ײ���©����������ֽ�����˳�ȥ���ܵ�MnO(OH)2��
II. ���ײ���©����������ֽ�����˳�ȥ���ܵ�MnO(OH)2��
![]() III. ���˵õ���KMnO4��Һ��������ɫ�Լ�ƿ���ڰ�����
III. ���˵õ���KMnO4��Һ��������ɫ�Լ�ƿ���ڰ�����
![]() IV. ����������ԭ�ζ���������700C��800C�������û��Լ������ȸߡ���Է��������ϴ��ȶ��ԽϺõ����ʣ�����ᾧ��H2C2O4•2H2O ����Һ�궨��Ũ�ȡ���֪�� MnO4- (H+)��Mn2+ �� H2C2O4 �� CO2 ��Ӧ������Ԫ��û�еá�ʧ���ӡ���ش��������⣺
IV. ����������ԭ�ζ���������700C��800C�������û��Լ������ȸߡ���Է��������ϴ��ȶ��ԽϺõ����ʣ�����ᾧ��H2C2O4•2H2O ����Һ�궨��Ũ�ȡ���֪�� MnO4- (H+)��Mn2+ �� H2C2O4 �� CO2 ��Ӧ������Ԫ��û�еá�ʧ���ӡ���ش��������⣺
![]() ��1��д���������ữ��������KMnO4 ��H2C2O4��Ӧ�����ӷ���ʽ�� ��
��1��д���������ữ��������KMnO4 ��H2C2O4��Ӧ�����ӷ���ʽ�� ��
![]() ��2����α�֤��700C��800C�����½��еζ������� ��
��2����α�֤��700C��800C�����½��еζ������� ��
![]() ��3��ȷ��ȡһ�������25.00 mL����KMnO4��Һʹ�õ������� ��
��3��ȷ��ȡһ�������25.00 mL����KMnO4��Һʹ�õ������� ��
![]() ��4����ȷ��ȡW g���Լ�����ˮ���500 mLˮ��Һ��ȡ25.00 mL������ƿ�У��ø��������Һ�ζ����յ㣬���ĸ��������ҺV mL���ʣ�
��4����ȷ��ȡW g���Լ�����ˮ���500 mLˮ��Һ��ȡ25.00 mL������ƿ�У��ø��������Һ�ζ����յ㣬���ĸ��������ҺV mL���ʣ�
![]() �ٵζ��յ��־�� ��
�ٵζ��յ��־�� ��
![]() ��KMnO4��Һ�����ʵ���Ũ��Ϊ mol?L��1��
��KMnO4��Һ�����ʵ���Ũ��Ϊ mol?L��1��
![]() ��5�����÷������ܵ�KMnO4����Һȥ�ζ�ˮ����Fe2����������õ�Ũ��ֵ�� -------���ƫ�ߡ���ƫ�͡���
��5�����÷������ܵ�KMnO4����Һȥ�ζ�ˮ����Fe2����������õ�Ũ��ֵ�� -------���ƫ�ߡ���ƫ�͡���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
KMnO4��Һ������������ԭ��Ӧ�ζ��ı�Һ������KMnO4��ǿ�����ԣ�������Һ�����ױ������л�ˮ��ijЩ��![]() ����ԭ�����ʻ�ԭ����������������MnO(OH)2���������KMnO4����Һ�IJ����ǣ�
����ԭ�����ʻ�ԭ����������������MnO(OH)2���������KMnO4����Һ�IJ����ǣ�
I. ��ȡ�Զ�����������KMnO4��������ˮ������Һ���Ȳ�������1 h��
II. ���ײ���©����������ֽ�����˳�ȥ���ܵ�MnO(OH)2��
III. ���˵õ���KMnO4��Һ��������ɫ�Լ�ƿ���ڰ�����
IV. ����������ԭ�ζ���������700C��800C�������û��Լ������ȸߡ���Է��������ϴ��ȶ��ԽϺõ����ʣ�����ᾧ��H2C2O4??2H2O ����Һ�궨��Ũ�ȡ���֪�� MnO4- (H+)��Mn2+ �� H2C2O4 �� CO2 ��Ӧ������Ԫ��û�еá�ʧ���ӡ���ش��������⣺
��1��д���������ữ��������KMnO4 ��H2C2O4��Ӧ�����ӷ���ʽ�� ��
��2����α�֤��700C��800C�����½��еζ������� ��
��3��ȷ��ȡһ�������25.00 mL����KMnO4��Һʹ�õ������� ��
��4����ȷ��ȡW g���Լ�����ˮ���500 mLˮ��Һ��ȡ25.00 mL������ƿ�У��ø��������Һ�ζ����յ㣬���ĸ������![]() ��ҺV mL���ʣ�
��ҺV mL���ʣ�
�ٵζ��յ��־�� ��
��KMnO4��Һ�����ʵ���Ũ��Ϊ mol��L��1��
��5�����÷������ܵ�KMnO4����Һȥ�ζ�ˮ����Fe2����������õ�Ũ��ֵ�� -------���ƫ�ߡ���ƫ�͡���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com