
(15分)【化学一一选修物质结构与性质】X、Y、Z、M、N、Q、P为元素周期表前四周期的7种元素。其中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量最高的元素,M的内层电子数是最外层电子数的9倍,N的原子序数比M小1,Q在元素周期表的各元素中电负性最大。P元素的第三电子层处于全充满状态,第四电子层只有一个电子。请回答下列问题:
(1)X元素在周期表中的位置是 ,它的外围电子的电子排布图为 。P元素属于 区元素,
(2)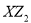 分子的空间构型是 ,
分子的空间构型是 ,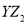 分子中Y的杂化轨道类型为 ,相同条件下两者在水中的溶解度较大的是 (写分子式),理由是 。
分子中Y的杂化轨道类型为 ,相同条件下两者在水中的溶解度较大的是 (写分子式),理由是 。
(3)含有元素N的盐的焰色反应为 色,许多金属盐都可以发生焰色反应,其因是 。
(4)元素M与元素Q形成晶体结构如图1所示设其晶胞边长为a pm,该化合物的摩尔质量为Dg/mol。求该晶胞密度的计算式为 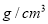
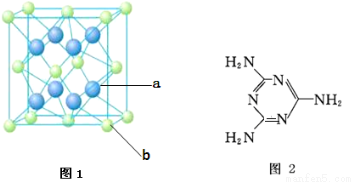
(5)三聚氰胺是一种含氮化合物,其结构简式如图2所示。三聚氰胺分子中氮原子轨道杂化类型是 ,1 mol三聚氰胺分子中o键的数目为 。
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源:2014-2015甘肃省天水市高二下学期第一次月考化学试卷(解析版) 题型:选择题
关于同分异构体的叙述正确的是
A.相对分子质量相同而结构不同的化合物互称为同分异构体
B.化学式相同而结构不同的化合物互称为同分异构体
C.同分异构体之间由于分子组成相同,所以它们的性质相同
D.只有少数的有机物之间存在同分异构现象
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省六校联盟高三第三次联考理科综合化学试卷(解析版) 题型:选择题
50℃时,0.1mol·L-1Na2CO3溶液pH=12,下列判断正确的是
A.c(OH-)=10-2mol·L-1
B.加入少量NaOH固体,c(Na+)和c(CO32-)均增大
C.c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-)
D.2c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省合肥市高三第二次教学质量检测理综化学试卷(解析版) 题型:填空题
(14分)硫代硫酸钠是一种常见的化工原料,将SO2通入按一定比例配成的Na2S和Na2CO3的混合溶液中,便可得到Na2S2O3,其制备反应方程式为:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2
(1)在配制混合溶液前先将蒸馏水加热煮沸一段时间后待用,其目的是 。
(2)用该方法获得的Na2S2O35H2O晶体中常混有一定量的杂质,某兴趣小组欲对其中所含杂质成分进行探究。
【提出假设】该晶体中含有的杂质可能是:Na2CO3、Na2SO3、_____、_____等中的一种或几种,若晶体中混有Na2SO3,则生成Na2SO3的化学方程式为 。
【判断与思考】
某同学取少量制得的晶体溶于足量稀硫酸,并将产生的气体通入CuSO4溶液中,未见黑色沉淀,据此认为晶体中一定不含Na2S,你认为其结论是否合理?_______ (填“合理”、“不合理”)并说明理由:______________
【设计方案进行实验】
若检验晶体中含Na2CO3,完成下表实验方案、现象及结论(仪器自选)。
限选实验试剂:3mol/LH2SO4、1mol/LNaOH酸性KMnO4溶液、饱和NaHCO3溶液、品红溶液、澄清石灰水

(3)已知:2 Na2S2O3+I2=2NaI+Na2S4O6。为测定所制得晶体的纯度,该小组以淀粉作指示剂,用0.010mol/L 的碘水进行多次取样滴定,测得Na2S2O35H2O的含量约为102%。若所用试剂及操作均无不当,产生该结果最可能的原因是______________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省合肥市高三第二次教学质量检测理综化学试卷(解析版) 题型:选择题
下列各反应对应的离子方程式正确的是
A.向Ca(OH)2溶液中加入过量的NaHCO3溶液Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O
B.向100 mL 0.12 mol/L-1的Ba(OH)2溶液中通入0.02 mol CO2:Ba2++3OH-+2CO2=HCO3-+BaCO3↓+H2O
C.硫酸氢钠与氢氧化钡两种溶液反应后pH恰好为7:H++SO42-+Ba2++OH-=BaSO4↓+H2O
D.向含0.1mol/LNaOH和0.1mol/LNa2CO3的溶液中加入1L0.4mol/L稀盐酸OH-+CO32-+3H+=CO2↑+2H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省上饶市高三上学期第一次联考化学试卷(解析版) 题型:选择题
有一种铁的“氧化物”样品,用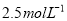 盐酸
盐酸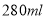 恰好完全溶解,所有溶液还能吸收标况下的0.56L氯气,如使其中的
恰好完全溶解,所有溶液还能吸收标况下的0.56L氯气,如使其中的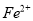 全部转化为
全部转化为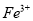 ,该样品可能的化学式是
,该样品可能的化学式是
A.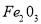 B.
B.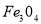 C.
C.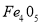 D.
D.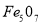
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省上饶市高三第二次高考模拟化学试卷(解析版) 题型:推断题
(15分,除标明外,其余每空2分)吡洛芬是一种用于治疗风湿病的药物。它的合成路线如下:

回答下列问题:
(1)B→C的反应类型为 。
(2)A→B的化学方程式为 。从整个合成路线看,步骤A→B的目的是 。
(3)E的结构简式为 。
(4)A在一定条件下可生成F( )。写出同时满足下列条件的F的两种同分异构体的结构简式: 。
)。写出同时满足下列条件的F的两种同分异构体的结构简式: 。
①属于芳香族化合物
②是一种α-氨基酸
③分子中有6种不同化学环境的氢原子
(5)非那西汀是一种解热药,其结构简式为 。写出以苯酚钠CH3CH2OH和(CH3CO)2O为原料制备非那西汀的合成路线流程图(无机试剂任用)。
。写出以苯酚钠CH3CH2OH和(CH3CO)2O为原料制备非那西汀的合成路线流程图(无机试剂任用)。
合成路线流程图示例如下:
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省无锡市高三期末考试化学试卷(解析版) 题型:填空题
(12分)锂/磷酸氧铜电池是一种以磷酸氧铜作为正极材料的锂离子电池,其正极的活性物质是Cu4O(PO4)2,制备流程如下:
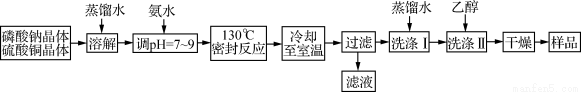
主要反应原理:2Na3PO4+4CuSO4+2NH3·H2O===Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)实验室进行“过滤”操作使用的玻璃仪器主要有________。
(2)流程中“洗涤Ⅰ”后,检验沉淀已洗涤干净的方法是____________________。
(3)该电池放电时,负极锂转化为Li2O,正极磷酸氧铜转变为Cu和Li3PO4,写出该电池放电时的化学方程式____________________。
(4)准确称取上述流程所得的样品38.56 g[假定样品中只含Cu4O(PO4)2和CuO两种物质],使其完全溶于一定量的硝酸中,再加入氢氧化钠溶液,使铜完全沉淀,将沉淀灼烧使其转变为黑色氧化铜,最终称得残留固体质量为27.20 g。计算所得样品中磷酸氧铜的质量分数。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省哈尔滨市高二下学期第一次月考化学试卷(解析版) 题型:填空题
(10分)(1)键线式 表示的分子式 ;
表示的分子式 ;
名称 。
(2)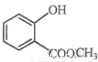 中含有的官能团的名称为 。
中含有的官能团的名称为 。
(3)写出下列物质的结构简式:
2,6-二甲基-4-乙基辛烷: 。
(4)写出该物质的名称: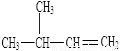 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com