
【题目】下列离子方程式表示正确的是 ( )
A. 往FeI2溶液中通入过量氯气:Cl2+2Fe2+===2Cl-+2Fe3+
B. 将明矾溶于水中生成胶体:Al3++3H2O![]() Al(OH)3(胶体)+3H+
Al(OH)3(胶体)+3H+
C. 大理石溶于醋酸中:CaCO3+2H+===Ca2++H2O+CO2↑
D. 铜与稀硝酸反应:3Cu+4H++2NO3-===3Cu2++2NO↑+2H2O
【答案】B
【解析】
A.因氧化性I2<Fe3+<Cl2,故通入过量氯气后溶液中的Fe2+和I-都被氧化,离子方程式为:4I-+3Cl2+2Fe2+=6Cl-+2Fe3++2I2,错误;
B.明矾成分为KAl(SO4)2·12H2O溶于水后,完全电离出Al3+,Al3+会发生水解生成Al(OH)3胶体,其离子方程式为Al3++3H2O![]() Al(OH)3(胶体)+3H+,正确;
Al(OH)3(胶体)+3H+,正确;
C.醋酸为弱电解质,书写离子方程式时不能拆分,故离子方程式为:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑,错误;
D.离子方程式中电荷不守恒,正确的离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,错误。


 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
【题目】某小组为研究电化学原理,设计如图装置,下列叙述不正确的是

A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铁片上发生的反应为: Fe2e===Fe2+
C. a和b用导线连接时,电子从Cu片流向铁片
D. a和b用导线连接时,Cu2+向铜电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将0.1mol/L的一元酸HA溶液逐滴滴加到10mL0.1mol/LNaOH溶液中,pH的变化曲线如图所示。下列说法错误的是

A. a点所示溶液中c(Na+)>c(A-)>c(OH-)>c(HA)
B. a、b两点所示溶液中水的电离程度a点大于b点
C. pH=7时,c(Na+)=c(A-)+c(HA)
D. 一元酸HA为弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。
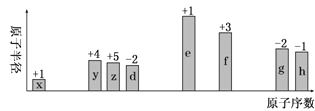
根据判断出的元素回答问题:
(1)z在周期表中的位置是_________________________________。
(2)写出x和d组成的一种四原子共价化合物的电子式_______________。
(3)y、g、h的最高价氧化物对应水化物的酸性最强的是______________(填化学式)。
(4)写出f的最高价氧化物与e的最高价氧化物对应的水化物反应的离子方程式______。
(5)已知e和g的最高价氧化物对应的水化物的稀溶液反应生成1mol水时所放出的热量为Q kJ。请写出该反应的中和热的热化学方程式___________。
(6)用y元素的单质与f元素的单质可以制成电极浸入由x、d、e三种元素组成的化合物的溶液中构成电池负极反应式为___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化铈(CeO2)是一种重要的稀土氧化物。以氟碳铈矿(主要含CeFCO3)为原料制备CeO2的一种工艺流程图如图:
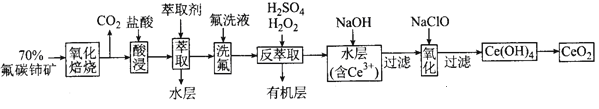
已知:①Ce4+既能与F-结合成[CeFX](4-x)+,也能与SO42-结合成[CeSO4]2+;
②在硫酸体系中Ce4+能被萃取剂[(HA)2]萃取,而Ce3+不能。
回答下列问题:
(1)“氧化焙烧”前需将矿石粉碎成细颗粒,其目的是_____。
(2)“酸浸”中会产生大量黄绿色气体,写出CeO2与盐酸反应的离子方程式_____,为避免上述污染,请提出一种解决方案:_____。
(3)“萃取”时存在反应:Ce4++n(HA)2![]() Ce·(H2n-4A2n)+4H+。实验室中萃取时用到的主要玻璃仪器名称为_____。
Ce·(H2n-4A2n)+4H+。实验室中萃取时用到的主要玻璃仪器名称为_____。
(4)“反萃取”中,在稀硫酸和H2O2的作用下CeO2转化为Ce3+,H2O2在该反应中作_____(填“催化剂”、“氧化剂”或“还原剂”),每有1molH2O2参加反应,转移电子物质的量为_____。
(5)“氧化”步骤的化学方程式为_____。
(6)取上述流程得到的CeO2产品0.50g,加硫酸溶解后,用0.10mol/L FeSO4标准溶液滴定至终点时(铈被还原为Ce3+,其他杂质均不参加反应),消耗25.00mL标准溶液。该产品中CeO2的质量分数为_____(Ce的相对原子质量为140)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~E是中学常见的5种化合物,A、B是氧化物,它们之间的转化关系如下图所示。则下列说法正确的是( )

A. X与A反应的化学方程式是:Al2O3 + 2Fe ![]() Fe2O3 + 2Al
Fe2O3 + 2Al
B. 检验D溶液中的金属阳离子的反应:Fe3++3SCN—= Fe(SCN)3↓
C. 单质Y在一定条件下能与水发生置换反应
D. 由于化合物B和C均既能与酸反应,又能与碱反应,所以均是两性化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某药物中间体的结构示意图:

试回答下列问题:
⑴观察上面的结构式与立体模型,通过对比指出结构式中的“Et”表示_______________;该药物中间体分子的化学式为_____________。
⑵解决有机分子结构问题的最强有力手段是核磁共振氢谱(PMR)。有机化合物分子中有几种化学环境不同的氢原子,在PMR中就有几个不同的吸收峰,吸收峰的面积与H原子数目成正比。
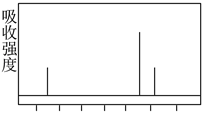
现有一种芳香族化合物与该药物中间体互为同分异构体,其模拟的核磁共振氢谱图如上图所示,试写出该化合物的结构简式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10mL0.1mol·L-1CuCl2溶液中滴入0.1ml·L-1的Na2S溶液,滴加过程中溶液中-1gc(Cu2+)随滴人的Na2S溶液体积的变化如图所示。下列叙述正确的是
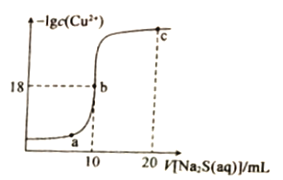
A. Na2S溶液中:c(S2-)+c(HS-)+c(H2S)==2c(Na+)
B. Ksp(CuS)的数量级为10-36
C. a、b、c三点溶液中,b点水的电离程度最大
D. c点溶液中:c(C1-)=2c(Na+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com