
分析 结合N=nNA、n=$\frac{m}{M}$计算.
解答 解:物质的量为$\frac{19.6g}{98g/mol}$=0.2mol,含有1.204×1023个分子,则阿伏加德罗常数为$\frac{1.204×1{0}^{23}}{0.2}$=6.02×1023 mol-1;agCO32-分子中含有b个电子,则阿伏加德罗常数可表示为$\frac{b}{\frac{a}{60}×32}$=$\frac{15b}{8a}$,
故答案为:6.02×1023 mol-1;$\frac{15b}{8a}$.
点评 本题考查物质的量的计算,为高频考点,把握质量、物质的量、微粒数的关系为解答的关键,侧重分析与计算能力的考查,注意基本计算公式的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g)△H=-1367.0 kJ•mol-1(燃烧热) | |
| B. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=+57.3 kJ•mol-1(中和热) | |
| C. | S(s)+O2(g)═SO2(g)△H=-269.8 kJ•mol-1(反应热) | |
| D. | 2H2(g)+O2(g)═2H2O(l)△H=571.6kJ•mol-1(反应热) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 200mL 2mol/L MgCl2溶液 | B. | 150mL 5mol/L KClO3溶液 | ||
| C. | 标准状况下,13.44L的HCl气体 | D. | 29.25gNaCl固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 没有明显变化 |
| ② | B+D | 有无色、无味气体生成 |
| ③ | B+C | 有白色沉淀生成 |
| ④ | A+D | 有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
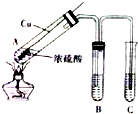 浓硫酸是一种重要的化工产品.
浓硫酸是一种重要的化工产品.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com