
| | 实验步骤 (画图表示,参照下图) | 实验现象 | 实验结论 |
| 非金属性递变 | | | |
| 金属性递变 | | | |
实验步骤 | 实验现象 | 实验结论 |
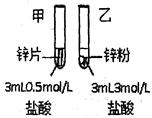 (锌片和锌粉的质量相同,盐酸均过量) | 均有气体生成,锌粉比锌片消失快。 | 反应物接触面积越大,反应速率越快 |
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源:不详 题型:实验题
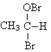
| 实验操作 | 预期现象与结论 |
| 步骤1:取一定量 B 于试管中,然后边震荡试管边慢慢加入适量 C 和 D 。 | |
| 步骤2:固定好装置,用酒精灯缓慢加热。将产生的蒸气通到 E 溶液的液面上。 | F , G 。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
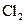 、
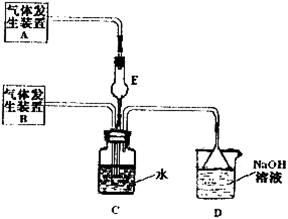
、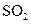 气体,现采用Na2SO3与70%的浓硫酸为原料制取SO2,采用MnO2和浓盐酸为原料制取C12。在此实验中,E仪器的作用是__________;发生装置B应选择以下三种装置中的___________(填序号)。
气体,现采用Na2SO3与70%的浓硫酸为原料制取SO2,采用MnO2和浓盐酸为原料制取C12。在此实验中,E仪器的作用是__________;发生装置B应选择以下三种装置中的___________(填序号)。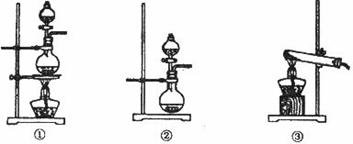
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 N2O4(g) 的平衡常数K=13.3,该条件下密闭容器中N2O4和NO2的混合气体达到平衡时c(NO2)="0.0300" mol·L-1。
N2O4(g) 的平衡常数K=13.3,该条件下密闭容器中N2O4和NO2的混合气体达到平衡时c(NO2)="0.0300" mol·L-1。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 入一种固体试剂,该试剂的名称为_________,B中能产生氨气和氧气混合气体的原
入一种固体试剂,该试剂的名称为_________,B中能产生氨气和氧气混合气体的原 因(结合化学方程式回答)_ __。
因(结合化学方程式回答)_ __。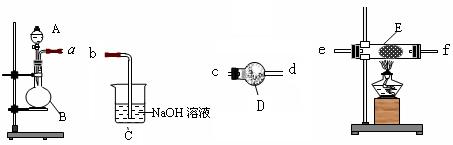
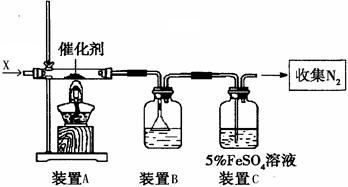
 4NO2(g);△H>0,下表为反应在某温度下的部分实验数据:
4NO2(g);△H>0,下表为反应在某温度下的部分实验数据:| t/s | 0 | 500 | 1000 |
| c(N2O3)/mol·L-1 | 5.00 | 3.52 | 2.48 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
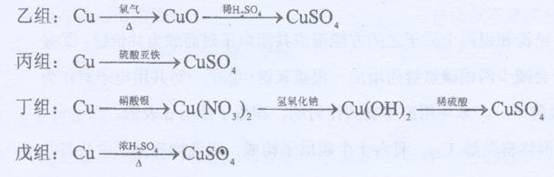
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 假设2:既不存在SO32-也不存在ClO-
假设2:既不存在SO32-也不存在ClO- ______
______ L-1H2SO4、1moL
L-1H2SO4、1moL L-1NaOH、0.01mol
L-1NaOH、0.01mol L-1KMnO4、淀粉-KI溶液、紫色石蕊试液.
L-1KMnO4、淀粉-KI溶液、紫色石蕊试液.| 实验步骤 | 预期现象和结论 |
步骤1:取少量吸收液于试管中,滴加3 moL L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中 L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中 |  |
| 步骤2: | |
| 步骤3: | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
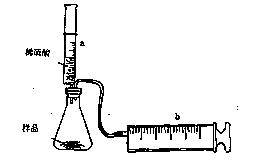 |
| | 50mL稀硫酸 | 50mL稀硫酸 | 50mL稀硫酸 |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(标况) | 2.24L | 3.36L | 3.36L |
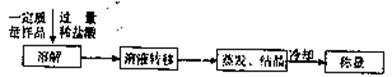
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com