
【题目】现代建筑的门窗框架常用电镀加工成的古铜色硬铝制造.取硬铝样品进行如图所示的实验(每一步试剂均过量),由此可推知,硬铝的组成为( ) 
A.Al、Cu、Mg、Si
B.Al、Mg、Si、Zn
C.Al、Fe、C,Cu
D.Al、Si、Zn、Na
【答案】A
【解析】解:A.样品中加入过量稀盐酸时,铝、镁完全和稀盐酸反应,铜、硅不能和稀盐酸反应,加入过量氢氧化钠溶液时,硅和氢氧化钠反应,而铜不能和氢氧化钠反应,故A正确;B.加入过量稀盐酸时,铝、镁和锌和稀盐酸完全反应,加入过量氢氧化钠溶液时,硅和氢氧化钠反应,没有不溶物,故B错误;
C.样品中加入过量稀盐酸时,铝、铁和稀盐酸完全反应,加入过量氢氧化钠溶液时,碳和铜不能和氢氧化钠反应,故C错误;
D.样品中加入过量稀盐酸时,铝、镁、锌和铁和稀盐酸完全反应,故D错误.
故选:A.
金属和酸溶液反应生成氢气,则比含有活泼性较强的金属,由于Si+2NaOH+H2O═Na2SiO3+2H2↑,所以在不溶物中加入过量的氢氧化钠溶液由气体生成,可推测有硅存在,最后剩余不溶物,则一定存在与盐酸、氢氧化钠都不反应的金属,以此解答该题.


科目:高中化学 来源: 题型:
【题目】把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含b mol BaCl2的溶液恰好使S完全沉淀;另一份加入含a mol NaOH的溶液,恰好使Mg2+完全沉淀。则原混合溶液中K+的浓度为( )
A. ![]() mol·L-1 B.
mol·L-1 B. ![]() mol·L-1 C.
mol·L-1 C. ![]() mol·L-1 D.
mol·L-1 D. ![]() mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质作用时,反应条件或反应物用量的改变,所得的产物的成分不会发生改变的是( )
A.固体Na2O2与CO2
B.氯气与NaOH溶液
C.Ba(OH)2溶液与SO2
D.饱和NaHCO3溶液与石灰水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mL碘的饱和溶液中加入5mL苯,充分混合后静置,实验现象为(( )
A. 液体分层,下层为紫色B. 液体分层,上层无色
C. 液体分层,下层无色D. 有固体沉淀析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物CH3﹣CH═CH﹣Cl不能发生的反应有( ) ①取代反应 ②加成反应 ③消去反应 ④使溴水褪色 ⑤使酸性KMnO4溶液褪色⑥与AgNO3溶液生成白色沉淀 ⑦聚合反应.
A.①②③④⑤⑥⑦
B.⑦
C.⑥
D.②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制100mL0.100mol/LNa2CO3溶液时,有下列步骤:①溶解②转移③定容④计算⑤称量⑥洗涤,正确的顺序为( )
A. ⑤④①⑥②③B. ⑤④②①⑥③
C. ④⑤①②⑥③D. ⑥④③⑤①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用少量的溴水和足量的乙醇制备1,2﹣二溴乙烷的装置如图所示: 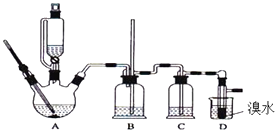
乙醇 | 1,2二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/gcm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | ﹣130 | 9 | ﹣116 |
请回答下列问题:
(1)写出制备1,2二溴乙烷的反应原理方程式:、
(2)在此制备实验中,要尽可能迅速地把反应温度升高到170℃左右,最主要的目的是(填序号).
a.引发反应 b.加快反应速度c.防止乙醇挥发 d.减少副产物乙醚生成
(3)装置B的作用是 .
(4)在装置C中应加入(填序号),其目的是吸收反应中可能生成的酸性气体.
a.水b.浓硫酸c.氢氧化钠溶液d.饱和碳酸氢钠溶液
(5)判断该制备反应已经结束的最简单方法是 .
(6)将1,2二溴乙烷粗产品置于分液漏斗中,加水振荡后静置,产物应在(填“上”或“下”)层.
(7)若产物中有少量副产物乙醚,可用的方法除去.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com