
 ,在周期表中的位置第四周期ⅢB族,属于d区.
,在周期表中的位置第四周期ⅢB族,属于d区. 分析 (1)按照从第一到第四周期的顺序,根据元素周期表中各元素结构及未成对电子数进行解答;
(2)根据Ga在元素周期表中是第四周期、第ⅢA族,原子序数是31及工作原理写出Ga原子的电子排布式;
(3)根据共用电子对偏向电负性大的原子进行解答;
(4)某元素原子共有3个价电子,其中一个价电子位于第三能层d轨道,价电子排布式为3d14s2,其基态原子核外电子排布式为:1s22s22p63s23p63d14s2,根据电子最后填入原子轨道确定分区,根据最大能层数确定周期,根据价电子数确定族序数.
解答 解:(1)第一周期中,有1个未成对电子的是氢原子,其电子排布式为1s1;第二周期中,未成对电子是2个的有两种分别为:C:1s22s22p2和O:1s22s22p4;第三周期中,未成对电子是3个的是P:1s22s22p63s23p3;第四周期中未成对电子是4个的是Fe:1s22s22p63s23p63d64s2,
故答案为:5;
(2)Ga在元素周期表中是第四周期、第ⅢA族,原子序数是31,即其原子核外电子数是31,根据核外电子的排布规律可以写出该原子的电子排布式为:1s22s22p63s23p63d104s24p1或[Ar]3d104s24p1,
故答案为:1s22s22p63s23p63d104s24p1或([Ar]3d104s24p1);
(3)共用电子对偏向电负性大的原子,CH4中共用电子对偏向C,则电负性C>H;SiH4中共用电子对偏向H,则电负性H>Si,所以C、Si、H的电负性大小关系为:C>H>Si,
故答案为:C>H>Si;
(4)某元素原子共有3个价电子,其中一个价电子位于第三能层d轨道,价电子排布式为3d14s2,其价电子排布图为: ;
;
其基态原子核外电子排布式为:1s22s22p63s23p63d14s2,最大能层数为4,说明位于第四周期,价电子排布式为3d14s2,说明位于第ⅢB族,所以该元素处于第四周期ⅢB族;
该元素的电子最后填入原子轨道为3d,因此处于周期表的d区,
故答案为: ;第四周期ⅢB族;d.
;第四周期ⅢB族;d.
点评 本题考查原子结构与元素周期律的关系、元素电负性大小比较,题目难度中等,注意掌握元素周期表结构、元素周期律的内容,明确原子的基态电子排布式的表示方法.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 一定不存在乙烯 | B. | 一定不存在甲烷 | C. | 一定存在甲烷 | D. | 一定存在乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定温度下,10mL 0.50mol•L-1NH4Cl溶液与20mL 0.25mol•L-1NH4C1溶液含NH4+物质的量相同 | |
| B. | 25℃时,将a mo1•L-l氨水与0.01 moI•L-1盐酸等体积混合,反应完全时溶液中c(NH4+)=c(C1-),用含a的代数式表示反应完全时NH3•H2O的电离常数Kb=$\frac{1{0}^{-9}}{a-0.01}$ | |
| C. | 某酸式盐NaHA溶液中一定有:c(OH-)+c(A2-)=c(H+)+c(H2A) | |
| D. | 等体积、pH都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性:HA>HB |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Na+、NO3-、Cl- | B. | Na+、NH4+、SO42-、Cl- | ||
| C. | Na+、K+、I-、NO3- | D. | Na+、K+、MnO4-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O与BeCl2为角形(V形) | B. | CS2与SO2为直线形 | ||
| C. | BF3与PCl3为三角锥形 | D. | SO3与CO${\;}_{3}^{2-}$为平面三角形 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
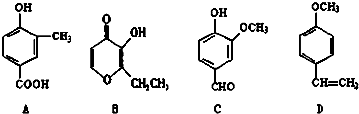
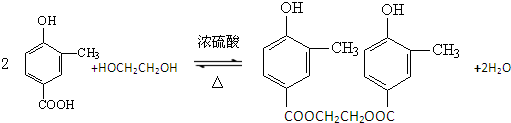 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大压强,单位体积活化分子数一定增加,化学反应速率一定增大 | |
| B. | 升高温度,活化分子百分数增加,化学反应速率一定增大 | |
| C. | 加入反应物,使活化分子百分数增加,化学反应速率增大 | |
| D. | 使用催化剂,一定降低了反应的活化能,化学反应速率一定增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KClO3在反应中得到电子 | |
| B. | ClO2是还原产物 | |
| C. | H2C2O4在反应中被还原 | |
| D. | 1molKClO3参加反应有1mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2FeO4中Fe为+6价,具有强氧化性,能杀菌消毒 | |
| B. | 反应①中,NaCl是氧化产物 | |
| C. | 反应①为氧化还原反应,反应②为复分解反应 | |
| D. | 若有2mol FeCl3发生反应,转移电子的物质的量为6mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com