
【题目】室温下,取m克铝镁合金与一定浓度的稀硝酸反应,合金恰好完全溶解(假定硝酸的还原产物只有NO),向反应后的混合溶液中滴加b mol/L NaOH溶液,当滴加到V mL时,得到沉淀质量恰好为最大值n克,则下列有关该实验的说法中正确的有( )
①沉淀中氢氧根的质量为(n﹣m)克
②恰好溶解后溶液中的NO3﹣离子的物质的量为![]() mol
mol
③反应过程中转移的电子数为![]() mol
mol
④生成NO气体的体积为![]() L
L
⑤发生反应的硝酸的物质的量为(![]() )mol
)mol
A. 2项 B. 3项 C. 4项 D. 5项
【答案】C
【解析】
①淀为Al(OH)3和Mg(OH)2,沉淀质量等于铝镁合金质量与氢氧根质量之和,所以沉淀中氢氧根的质量为(n-m)克,正确;②恰好溶解后溶液中的NO3﹣离子的物质的量等于沉淀质量最大时溶液中NO3﹣离子的物质的量,当沉淀量最大时,溶液中的溶质只有NaNO3,NO3﹣离子与Na+的物质的量相等,n(NO3﹣)=n(Na+)=n(NaOH)=![]() ,正确;③至沉淀量最大,生成的n克沉淀为Al(OH)3和Mg(OH)2。根据质量守恒定律,其中镁、铝元素的质量等于m克合金的质量,所以沉淀中氢氧根的质量为(n-m)克,在沉淀中,氢氧根的物质的量等于Mg2+、Al3+所带电荷的物质的量,也等于合金失去电子的物质的量,即为反应过程中转移的电子的物质的量,n(e-)=n(OH-)=
,正确;③至沉淀量最大,生成的n克沉淀为Al(OH)3和Mg(OH)2。根据质量守恒定律,其中镁、铝元素的质量等于m克合金的质量,所以沉淀中氢氧根的质量为(n-m)克,在沉淀中,氢氧根的物质的量等于Mg2+、Al3+所带电荷的物质的量,也等于合金失去电子的物质的量,即为反应过程中转移的电子的物质的量,n(e-)=n(OH-)=![]() ,正确;④根据电子守恒原理,生成NO时,HNO3中+5价的N原子得3个电子,因此生成NO的物质的量应该是转移电子的三分之一,即
,正确;④根据电子守恒原理,生成NO时,HNO3中+5价的N原子得3个电子,因此生成NO的物质的量应该是转移电子的三分之一,即![]() ,其体积在标准状况下为
,其体积在标准状况下为![]() ,但是选项中没有说明所处状态,则此时的体积不能确定,错误;⑤参加反应的HNO3有两种作用,起氧化剂和酸的作用,作为酸的HNO3(生成硝酸盐)的物质的量等于NaNO3的物质的量:
,但是选项中没有说明所处状态,则此时的体积不能确定,错误;⑤参加反应的HNO3有两种作用,起氧化剂和酸的作用,作为酸的HNO3(生成硝酸盐)的物质的量等于NaNO3的物质的量:![]() ,作氧化剂的HNO3的物质的量等于NO的物质的量为
,作氧化剂的HNO3的物质的量等于NO的物质的量为![]() ,所以与合金反应的HNO3的物质的量为
,所以与合金反应的HNO3的物质的量为![]() ,正确。故①②③⑤4项正确。答案选C。
,正确。故①②③⑤4项正确。答案选C。


科目:高中化学 来源: 题型:
【题目】某学生的实验报告所列出的下列数据中合理的是( )
A.用10mL量筒量取 7.13 mL稀盐酸
B.用托盘天平称量 25.20gNaCl
C.用广泛pH试纸测得某溶液的pH为 2.3
D.用25 mL滴定管做中和滴定时,用去某浓度的碱溶液 21.70 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究用CO2来生产燃料甲醇的反应原理,现进行如下实验:在体积为1 L的密闭容器中,充入1 mol CO2和3 molH2,一定条件下发生反应:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,T温度下,测得CO2和CH3OH(g)的浓度随时间变化如下图。请回答下列问题:
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,T温度下,测得CO2和CH3OH(g)的浓度随时间变化如下图。请回答下列问题:
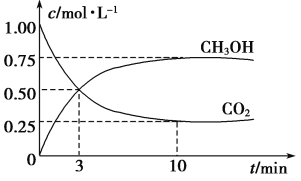
(1) 达平衡时,氢气的平衡浓度为C(H2)= 。
(2) 能够说明该反应已达到平衡的是 (填字母序号,下同)。
A.恒温、恒容时,容器内的压强不再变化
B.恒温、恒容时,容器内混合气体的密度不再变化
C.一定条件下,CO、H2和CH3OH的浓度保持不变
D.一定条件下,单位时间内消耗3 mol H2的同时生成1 mol CH3OH
(3)下列措施中能使平衡混合物中![]() 增大的是______________。
增大的是______________。
A.加入催化剂 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.降低温度
(4) 求此温度(T)下该反应的平衡常数K = 。若开始时向该1 L密闭容器中充入1 mol CO2,2molH2,1.5mol CH3OH和1 mol H2O(g),则反应向 (填“正”或“逆”)反应方向进行。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蔬菜、水果中富含纤维素,纤维素被食入人体后的作用是
A. 为人体内的化学反应提供原料
B. 为维持人体生命活动提供能量
C. 加强胃肠蠕动,具有通便功能
D. 人体中没有水解纤维素的酶,所以纤维素在人体中没有任何作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为四种短周期元素。X原子最外层电子数是核外电子层数的3倍;Y最高正价与最低负价的代数和为6;Z在地壳中的含量仅次于氧;Y、Z、W同周期,W的常见化合价为+3。回答下列问题:
(1)Y元素简单离子的结构示意图为 。
(2) Y与Z相比,非金属性强的是 (写元素符号)。下列事实能证明这一结论的是 。
A.常温下Y的单质呈气态,而Z的单质呈固态。
B.气态氢化物的稳定性Y比Z强。
C.Y与Z形成的化合物中,Z的化合价呈正价。
(3)Z在元素周期表中的位置是 。Z的最高价氧化物与Z同主族的单质A能发生置换反应,这个反应在工业上是获得Z的一步重要反应。写出该步反应的化学方程式,并标出电子转移的方向与数目 。
(4)向WY3溶液中加入足量的NaOH溶液,反应的离子方程式为 。
(5)ZX2中存在的化学键为 (填“离子键”或“共价键”),它的用途很广泛,请写出它的一个用途 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有1.92g铜投入一定量的浓硝酸中,铜完全溶解,生成的气体颜色越来越浅,共收集到标准状况下的气体672mL,将盛有该气体的容器倒扣在水中,通入标准状况下一定体积的氧气,恰好使气体完全溶于水中,则通入氧气的体积是( )
A. 168mL B. 224mL C. 504mL D. 336mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是( )
A. 人类目前所直接利用的能源大部分是由化学反应产生的
B. 煤,石油,天然气是当今世界最重要的三种化石燃料
C. 最理想的能源是煤炭
D. 人体运动所消耗的能量与化学反应有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为提纯下列物质<括号内为杂质)选用的试剂和分离方法部正确的是
物质 | 试剂 | 分离方法 | |
① | CuCl2(FeCl3) | CuO | 过滤 |
② | Cl2(HCl) | 饱和碳酸氢钠溶液 | 洗气 |
③ | 乙醇(水) | 金属钠 | 蒸馏 |
④ | NaCl溶液(Na2S) | AgCl | 过滤 |
A. ①③ B. ①④ C. 只有② D. ③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com