

(Ⅰ)
H2(g)+I2(g)![]() 2HI(g)(正反应为放热反应)
2HI(g)(正反应为放热反应)
该反应的化学平衡常数表达式为K=![]() ,反应各物质的浓度随时间变化情况如图(Ⅰ):
,反应各物质的浓度随时间变化情况如图(Ⅰ):
(1)根据图(Ⅰ)数据,反应开始至达到平衡时,平均速率v(HI)为_______________。
(2)反应达到平衡后,第8分钟时:
①若升高温度,化学平衡常数K______________。(填增大、减小或不变)
HI浓度的变化正确的是______________。(用图(Ⅱ)中a—c的编号作答)
②若加入I2,H2浓度的变化正确的是_______________。(用图(Ⅱ)中d—f的编号作答)
(3)反应达到平衡后,第8分钟时,若把容器的容积扩大一倍,请在图(Ⅲ)中画出8分钟后HI浓度的变化情况。

(Ⅱ)
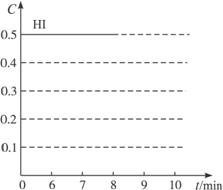
(Ⅲ)
解析:本题考查可逆反应的相关知识点。(1)根据图Ⅰ,找出3 min达到平衡时,![]()
(2)①升高温度时,由于正反应是放热反应,所以平衡向逆反应方向移动,生成物浓度减小,反应物浓度增大,所以化学平衡常数K减小,HI浓度减小,所以为c。②在体积不变的容器中,若加入I2,平衡将向正反应方向移动,H2的浓度将减小,所以为f。
(3)反应达到平衡后,第8 min时,若反应容器的容积扩大一倍,由于可逆反应前后气体的物质的量不变,所以平衡不动,只是浓度都减半,速率都减半而已。所以在8 min之前,浓度为0.5 mol·L-1,8 min之后,浓度为0.25 mol·L-1,见图。
答案:(1)0.167 mol·L-1·min-1
(2)①减小 c ②f
(3)见下图



科目:高中化学 来源: 题型:
A.反应放出的热量为0.
B.达平衡时H2O和CO的转化率相等
C.若将容器的体积压缩为
D.判断该反应达到平衡的依据是CO、H2O、CO2、H2的浓度都相等
查看答案和解析>>
科目:高中化学 来源: 题型:
在某一容积为2 L的密闭容器内,加入0.8 mol的H2和0.6 mol的I2,在一定的条件下发生如下反应:
H2(g)+I2(g)![]() 2HI(g)+Q(Q>0)
2HI(g)+Q(Q>0)
反应中各物质的浓度随时间变化情况如图1:

图1
(1)根据图1数据,反应开始至达到平衡时,平均速率v(HI)为______________________。
(2)反应达到平衡后,第8分钟时:
①若升高温度,化学平衡常数K________________(填写“增大”“减小”或“不变”),HI浓度的变化正确的是_________________(用图2中a—c的编号回答)。

图2
②若加入I2,H2浓度的变化正确的是________________(用图2中d—f的编号回答)。
(3)反应达到平衡后,第8分钟时,若把容器的容积扩大一倍,请在图3中画出8分钟后HI浓度的变化情况。

图3
查看答案和解析>>
科目:高中化学 来源:2013届新疆农七师高中高二上学期第一次阶段考试化学试卷(解析版) 题型:选择题
.已知在一定条件下有CO(g)+H2O(g)
 CO2(g)+H2(g),在某一容积为2 L的密闭容器中,加入0.2 mol的CO和0.2 mol的H2O,在催化剂存在的条件下,高温加热,发生如下反应:CO(g)+H2O(g)
CO2(g)+H2(g),在某一容积为2 L的密闭容器中,加入0.2 mol的CO和0.2 mol的H2O,在催化剂存在的条件下,高温加热,发生如下反应:CO(g)+H2O(g)  CO2(g)+H2(g) ΔH=a kJ/mol,反应达平衡后,测得c(CO)∶c(CO2)=3∶2,下列说法正确的是
CO2(g)+H2(g) ΔH=a kJ/mol,反应达平衡后,测得c(CO)∶c(CO2)=3∶2,下列说法正确的是
A.反应放出的热量为0.04a KJ
B.平衡时H2O的转化率为40%
C.若将容器的体积压缩为1 L,有利于该反应平衡正向移动
D.判断该反应达到平衡的依据是CO、H2O、CO2、H2的浓度都相等
查看答案和解析>>
科目:高中化学 来源:2010年河北省高一第二学期期中考试化学(理)试题 题型:选择题
在某一容积为2 L的密闭容器内,加入2 mol的CO和2 mol的H2O,高温加热,发生如下反应:CO(g) +H2O(g) CO2(g) + H2(g);1molCO完全反应放热a kJ。反应达到平衡后,测得n(CO2)=
0.8mol下列说法正确的是(
)
CO2(g) + H2(g);1molCO完全反应放热a kJ。反应达到平衡后,测得n(CO2)=
0.8mol下列说法正确的是(
)
A.判断该反应达到平衡的依据是CO、H2O、CO2、H2的浓度都相等
B.反应放出的热量为0.4a kJ
C.平衡时H2O 的转化率为40%
D.加入催化剂可以反应加快,放热更多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com