
【题目】Ⅰ: SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。
(1)SCR(选择性催化还原)工作原理:

① 尿素[CO(NH2)2]水溶液热分解为NH3和CO2,当燃油中含硫量较高时,尾气中SO2在O2作用下会形成(NH4)2SO4,使催化剂中毒。用化学方程式表示(NH4)2SO4的形成:________________________。
② 尿素溶液浓度影响NO2的转化,测定溶液中尿素(M=60 g·mol 1)含量的方法如下:取a g尿素溶液,将所含氮完全转化为NH3,所得NH3用过量的v1 mL c1 mol·L1 H2SO4溶液吸收完全,剩余H2SO4用v2 mL c2 mol·L1 NaOH溶液恰好中和,则尿素溶液中溶质的质量分数是________。
(2)NSR(NOx储存还原)工作原理:NOx的储存和还原在不同时段交替进行,如图a所示。

用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,该过程分两步进行,图b表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的Ba(NO3)2与H2的物质的量之比是__________。
Ⅱ:H2S和SO2会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,回答下列方法中的问题。
【ⅰ】H2S的除去: 方法1:生物脱H2S的原理为:
H2S+Fe2(SO4)3![]() S↓+2FeSO4+H2SO4
S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4![]() 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
(1)硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,由图3和图4判断使用硫杆菌的最佳条件为______________。

方法2:在一定条件下,用H2O2氧化H2S
(2)随着参加反应的n(H2O2)/n(H2S)变化,氧化产物不同。当n(H2O2)/n(H2S)=4时,氧化产物的分子式为__________。
【ⅱ】SO2的除去:(双减法):用NaOH吸收SO2,并用CaO使NaOH再生
NaOH溶液![]() Na2SO3溶液
Na2SO3溶液
(3)写出过程①的离子方程式:____________________;
【答案】 2SO2+O2+4NH3+2H2O=2(NH4)2SO4 ![]() 1∶8 30 ℃、pH=2.0 H2SO4 2OH+SO2
1∶8 30 ℃、pH=2.0 H2SO4 2OH+SO2![]()
![]() +H2O
+H2O
【解析】Ⅰ:(1)①SO2在O2作用下与NH3、H2O反应形成(NH4)2SO4,此反应中二氧化硫是还原剂,氧气是氧化剂,结合电子守恒和原子守恒可得此反应的化学方程式为2SO2+O2+4NH3+2H2O=2(NH4)2SO4;②吸收NH3的硫酸的物质的量为v1![]() 10-3L
10-3L![]() c1mol/L- v2
c1mol/L- v2![]() 10-3L
10-3L![]() c2mol/L
c2mol/L![]() =(c1v1-
=(c1v1-![]() c2v2)
c2v2)![]() 10-3mol/L,尿素的物质的量为
10-3mol/L,尿素的物质的量为![]() (c1v1-
(c1v1-![]() c2v2)
c2v2)![]() 10-3mol,则尿素溶液中溶质的质量分数是[
10-3mol,则尿素溶液中溶质的质量分数是[![]() (c1v1-
(c1v1-![]() c2v2)
c2v2)![]() 10-3mol×60g/mol
10-3mol×60g/mol![]() ag×100%=
ag×100%=![]() %];(2)由图示可知,第一步反应为H2与Ba(NO3)2作用生成NH3,每摩Ba(NO3)2作用生成NH3共转移16mol电子,根据电子守恒,参加反应的氢气的物质的量为
%];(2)由图示可知,第一步反应为H2与Ba(NO3)2作用生成NH3,每摩Ba(NO3)2作用生成NH3共转移16mol电子,根据电子守恒,参加反应的氢气的物质的量为![]() =8mol,则消耗的Ba(NO3)2与H2的物质的量之比是1: 8;
=8mol,则消耗的Ba(NO3)2与H2的物质的量之比是1: 8;
Ⅱ:(1)根据图3可知,温度30℃左右时,氧化速率最大,根据图4可知,PH=2.0时氧化速率最大,所以使用硫杆菌的最佳条件为30℃、PH=2.0;若反应温度过高,硫杆菌蛋白质变性失去活性造成反应速率下降;(2)根据化合价升降,当n(H2O2)/n(H2S)=4时,4molH2O2转移8mol电子,则1molH2S也转移8mol电子,化合价从-2价升高到+6价,所以氧化产物为H2SO4;(3)过程① 是NaOH与SO2的反应,反应离子方程式为:2OH+SO2![]()
![]() +H2O。
+H2O。


科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑩在表中的位置,回答下列问题:
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ||
3 | ⑧ | ⑨ | ⑩ |
(1)自然界物质种类最多的元素在周期表中的位置是____________________。
(2) ⑧⑨⑩的离子半径由大到小的顺序为__________________________(填化学用语)。
(3)写出由⑥⑧⑩元素形成的一种离子化合物的电子式:________________________。
(4)根据对角线元素性质相似规则,写出②的最高价氧化物对应的水化物与盐酸反应的离子方程式:__________________________________________________。
(5)③的氧化物、氢氧化物有两性,写出③的单质与⑧的最高价氧化物对的水化物反应的离子方程式:___________________________________________________________。
(6)已知![]() 分别是由①⑤⑥三种元素中的两种形成的10电子粒子,写出该反应式:________________________________________________。
分别是由①⑤⑥三种元素中的两种形成的10电子粒子,写出该反应式:________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们在远距离运输果实或花朵时,装有果实或花朵的密闭容器中,常常放有浸泡过KMnO4(aq)的硅土,其作用是
A.给容器消毒 B.杀死果实周围的细菌,防止霉变
C.延长果实或花朵的寿命 D.催熟果实或花朵
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质能发生消去反应且产物只有一种的是
A. (CH3)3COH B. CH3OH C. CH3CHICH2CH3 D. (CH3)3C-CH2Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中石化于2012年将年产120万吨的乙烯工程落户大庆,乙烯是有机化工工业的重要原料,有很多重要用途。如:乙烯催化氧化成乙醛可设计成如下图所示的燃料电池,在制备乙醛的同时还可获得电能,其总反应化学方程式为:2CH2=CH2+O2→2CH3CHO。下列有关说法正确的是
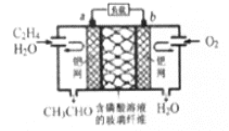
A. 该电池电极a为正极,b为负极
B. 电子移动方向:电极a→磷酸溶液→电极b
C. 负极反应式为:CH2=CH2-2e-+H2O=CH3CHO+2H+
D. b电极有2.24LO2反应,溶液中有0.4molH+迁移到b电极上反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国药学家屠呦呦作为抗疟新药青蒿素的第一发明人荣获2015年诺贝尔生理学或医学奖。青蒿素和双氢青蒿素的结构简式如图所示,下列说法错误的是

A.青蒿素易溶于苯,难溶于水
B.由青蒿素制备双氢青蒿素的反应属于还原反应
C.青蒿素可与NaOH溶液在一定条件下发生水解反应
D.双氢青蒿素的同分异构体不可能有芳香族化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“西气东输”中的“气”指天然气,其主要成分的化学式是________,结构式是__________。一定量的该气体燃烧过程的能量变化如图所示,从图中可以读出E1______E2(填“>”或“<”),该反应_______ (填“放出”或“吸收”)能量。
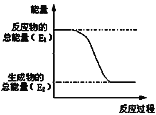
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以稀硫酸为电解质溶液,利用太阳能将CO2转化为低碳烯烃,工作原理图如下。下列说法正确的是

A. a电极为太阳能电池的正极
B. 产生丙烯的电极反应式为:3CO2+18H++18e-===CH3CH=CH2+6H2O
C. 装置中每转移2e-,理论上有2molH+通过质子交换膜从左向右扩散
D. 太阳能电池的原理与原电池的原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
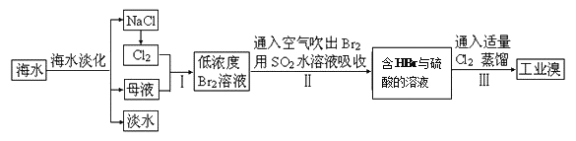
【题目】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
(1)除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序正确的是__________。
A.NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
B.BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸
C.NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤后加盐酸
D.Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
(2)制备钠单质的方法之一是将熔融NaCl进行电解,写出电解化学方程式:
______________________________________________________。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是____________。写出步骤Ⅱ中发生反应的化学方程式:_______________________________________________。
(4)某化学小组的同学为了了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59 ℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如下实验装置:
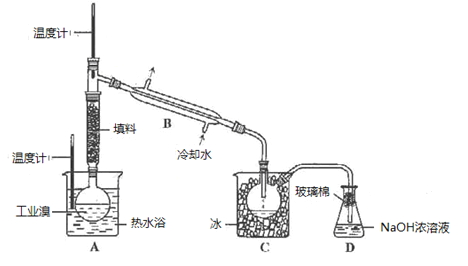
①图中仪器B的名称是________,冷却水的出口为____(填“甲”或“乙”)。
②C中液体的颜色为__________________。
③D装置的作用是__________________。
(5)已知某溶液中Cl-、Br-、I-的物质的量之比为2∶3∶4,现欲使溶液中的Cl-、Br-、I-的物质的量之比变成4∶3∶2,那么要通入Cl2的物质的量是原溶液中I-的物质的量的________。(填选项)
A.![]() B. C.
B. C.![]() D.
D.![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com