
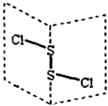
 S2Cl2是广泛用于橡胶工业的硫化剂,常温下S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体,其结构如图所示.下列说法错误的是( )
S2Cl2是广泛用于橡胶工业的硫化剂,常温下S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体,其结构如图所示.下列说法错误的是( )| A、S2Cl2的结构中各原子都达到了八电子稳定结构 |
| B、S2Br2与S2Cl2结构相似,熔沸点S2Br2>S2Cl2 |
| C、S2Cl2分子中的S为+1价,是含有极性键和非极性键的非极性分子 |
| D、S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O═SO2↑+3S↓+4HCl |
 ,每个原子周围都满足8电子稳定结构,故A正确;
,每个原子周围都满足8电子稳定结构,故A正确;

科目:高中化学 来源: 题型:
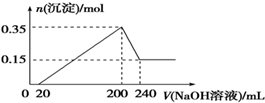 通过计算得到:
通过计算得到:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O2与CO2反应时,Na2O2是氧化剂,CO2是还原剂 |
| B、1mol过氧化钠中阴离子数目为1NA |
| C、过氧化钠与木炭、铝粉反应时,过氧化钠均表现出强氧化性 |
| D、过氧化钠与二氧化硫反应时可生成硫酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、该反应的平衡常数表达式K=
| ||
| B、若容器内气体的密度或压强保持不变,均说明该反应已达到平衡状态 | ||
| C、若Fe3O4足量,改变起始充入H2的浓度,达平衡时H2的转化率不变 | ||
| D、若初始时投入4.64g Fe3O4与一定量H2,反应达平衡时容器内固体共有4g,则Fe3O4的转化率为50% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu2+、NH4+、SO42-、OH- |
| B、Ag+、NO3-、Cl-、K+ |
| C、H+、Al3+、NO3-、Cl- |
| D、H+、Na+、NO3-、Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
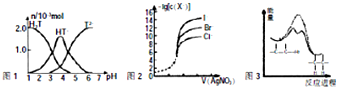
| A、常温下,向20mL 0.1mol?L-1酒石酸(H2T)溶液中添加0.1mol?L-1 NaOH溶液,有关微粒的物质的量与混合溶液的pH关系如图1,则H2T的酸性比H2CO3强 |
| B、用0.0100mol?L-1硝酸根标准溶液,滴定浓度均为0.100mol?L-1的Cl、Br及I的混合溶液,由图2曲线可确定首先沉淀的是Cl- |
| C、碳酸氢钠溶液中存在:c(H+)+2c(H2CO3)=c(OH-)+2c(CO32-) |
| D、由图3可说明烯烃与H2加成反应,虚线表示在催化剂的作用下进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaCO3和KHCO3 |
| B、Na2CO3和NaHCO3 |
| C、Na2CO3和K2CO3 |
| D、Na2CO3和CaCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④ | B、①②④⑥ |
| C、①②⑤⑥ | D、③④⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com