
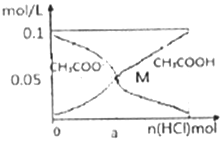
 常温下向l0mL0.1mol•L-1CH3COONa溶液中,不断通入HCl气体后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液休积变化),下列说法不正确的是( )
常温下向l0mL0.1mol•L-1CH3COONa溶液中,不断通入HCl气体后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液休积变化),下列说法不正确的是( )| A. | 当n(HCl)=1.0×10-3mol时,溶液中 c(Na+)=c(Cl-)>c(H+)>c(CH3COO-)>c(OH-) | |
| B. | M点溶液中水的电离程度比原溶液小 | |
| C. | 随着HCl的通入,c(OH-)/c(CH3COO-) 值不断减小 | |
| D. | 在M 点时,c(H+)-c(OH-)=(a-0.05)mol/L |
分析 l0mL0.1mol•L-1CH3COONa溶液中,CH3COONa的物质的量为n(CH3COONa)=0.1mol/L×10×10-3L=1×10-3mol/L,发生的反应为:CH3COONa+HCl═CH3COOH+NaCl,结合溶液中的守恒思想,据此分析判断.
解答 解:l0mL0.1mol•L-1CH3COONa溶液中,CH3COONa的物质的量为n(CH3COONa)=0.1mol/L×10×10-3L=1×10-3mol/L,发生的反应为:CH3COONa+HCl═CH3COOH+NaCl,
A.当n(HCl)=1.0×10-3mol时,恰好为化学计量点,反应恰好生成CH3COOH和NaCl,物质的量浓度为1:1的关系,此时溶液为酸性,由于CH3COOH是弱酸,则溶液中c(H+)>c(CH3COO-)>c(OH-),根据物料守恒,c(Na+)=c(Cl-),总的来说,溶液中 c(Na+)=c(Cl-)>c(H+)>c(CH3COO-)>c(OH-),故A正确;
B.M点时,溶液中c(CH3COOH)=c(CH3COONa),原溶液只存在CH3COONa,CH3COONa水解促进水的电离,CH3COOH存在抑制水的电离,所以M点溶液中水的电离程度比原溶液小,故B正确;
C.CH3COO-的水解平衡常数为Kb=$\frac{c(O{H}^{-})•c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$=$\frac{{K}_{w}}{{K}_{a}(C{H}_{3}COOH)}$,则溶液中$\frac{c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-})}$=$\frac{{K}_{w}}{{K}_{a}(C{H}_{3}COOH)c(C{H}_{3}COOH)}$,随着HCl的通入,溶液中c(CH3COOH)增大,则$\frac{c(O{H}^{-})}{c(C{H}_{3}COOH)}$不断减小,故C正确;
D.M点时,此时通入的HCl物质的量为amol,则c(Cl-)=$\frac{a}{10}$mol,c(Na+)=0.1mol/L,根据电荷守恒,c(Na+)+c(H+)=c(OH-)+c(CH3COO-)+c(Cl-),则c(H+)-c(OH-)=c(Cl-)+c(CH3COO-)-c(Na+),此时溶液中c(CH3COOH)=c(CH3COO-)=0.05mol/L,则c(H+)-c(OH-)=(0.05-$\frac{9}{10}$a)mol/L,故D错误.
故选D.
点评 本题考查滴定原理,明确滴定反应的过程,注意图象反应的是平衡浓度,牢牢把握溶液中的守恒思想,知道酸存在抑制水的电离,盐类水解促进水的电离,为高频考点,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| 表述1 | 表述2 | |
| A | 在水中,NaCl的溶解度比I2的溶解度大 | NaCl晶体中Cl-与Na+间的作用力大于碘晶体中分子间的作用力 |
| B | 通常条件下,CH4分子比PbH4分子稳定性高 | Pb的原子半径比C的大,Pb与H之间的键能比C与H间的小 |
| C | 同一主族的元素在形成化合物时,化合价一定均相同 | 同一主族元素原子的最外层电子数相同 |
| D | P4O10、C6H12O6溶于水后均不导电 | P4O10、C6H12O6均属于共价化合物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/s | 0 | 1 | 2 | 3 | 4 |
| c(NO)/mol•L-1 | 9.50×10-3 | 4.50×10-3 | 2.50×10-3 | 1.50×10-3 | 1.50×10-3 |
| c(CO)/mol•L-1 | 9.00×10-3 | 4.00×10-3 | 2.00×10-3 | 1.00×10-3 | 1.00×10-3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 以熔融CaF2-CaO作电解质,用下图所示袋置获得金属钙,并用钙还原TiO2制备金属钛.下列说法正确的是( )
以熔融CaF2-CaO作电解质,用下图所示袋置获得金属钙,并用钙还原TiO2制备金属钛.下列说法正确的是( )| A. | 整套装置工作前后中CaO的总量基本不变 | |
| B. | 阳极的电极反应式为2Ca2++4e-=2Ca | |
| C. | 石墨电极作阳极,质量不变 | |
| D. | 电解过程中,F-和O2-向阴极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 向溴化银悬浊液中加入溴化钠溶液,溴化银的Ksp减小 | |
| B. | 图中a点对应的是不饱和溶液 | |
| C. | 向c点对应的溶液中加入少量0.1 mol•L-1 AgNO3溶液,则c(Br-)增大 | |
| D. | 升高温度可以实现c点对应的溶液到b点对应的溶液的转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对于同一个化学反应,无论是一步完成还是分几步完成,其反应的焓变相同 | |
| B. | 等质量的硫蒸气和固态硫单质分别完全燃烧,后者放出的热量多 | |
| C. | 表示氢气燃烧热的△H为-285.8 kJ•mol-1,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ•mol-1 | |
| D. | 已知中和热△H为-57.3 kJ•mol-1,若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量等于57.3 kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com