
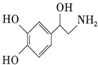
| A. | 每个去甲肾上腺素分子中含有3个酚羟基 | |
| B. | 去甲肾上腺素属于氨基酸 | |
| C. | 1mol去甲肾上腺素最多能与2molBr2发生取代反应 | |
| D. | 去甲肾上腺素既能与盐酸反应,又能与氢氧化钠溶液反应 |
分析 该分子中含有酚羟基、醇羟基、氨基和苯环,具有酚、醇、胺及苯的性质,能发生取代反应、氧化反应、还原反应、加成反应、取代反应等,据此分析解答.
解答 解:A.只有直接连接苯环的羟基才能酚羟基,所以该分子中含2个酚羟基、1个醇羟基,故A错误;
B.该分子中没有羧基,有氨基,故不叫氨基酸,故B错误;
C.苯环上酚羟基邻对位氢原子能被溴取代,且以1:1所以,所以1mol去甲肾上腺素最多能与3molBr2发生取代反应,故C错误;
D.含有酚羟基,具有酸性,含有氨基,具有碱性,所以去甲肾上腺素既能与盐酸反应,又能与氢氧化钠溶液反应,故D正确;
故选D.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系即可解答,侧重考查酚、醇和胺的性质,注意苯环上酚羟基邻对位氢原子才能和溴原子发生取代反应,注意酚羟基和醇羟基的区别.


科目:高中化学 来源: 题型:解答题
 大型飞机的发动机被誉为航空工业皇冠上的“宝石”.制造过程中通常采用碳化钨做关键部位的材料
大型飞机的发动机被誉为航空工业皇冠上的“宝石”.制造过程中通常采用碳化钨做关键部位的材料查看答案和解析>>
科目:高中化学 来源: 题型:选择题
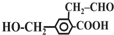 ,它在一定条件下可能发生的反应有 ①加成 ②水解 ③酯化 ④银镜反应 ⑤中和 ⑥消去 ⑦缩聚 其中正确的是( )
,它在一定条件下可能发生的反应有 ①加成 ②水解 ③酯化 ④银镜反应 ⑤中和 ⑥消去 ⑦缩聚 其中正确的是( )| A. | ②③④⑦ | B. | ①③⑤⑥ | C. | ①③④⑤⑦ | D. | ①③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
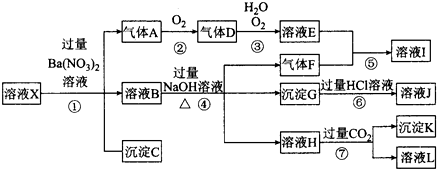
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 40K和40Ca 具有相同的中子数 | |
| B. | 40K+和40Ca2+ 具有相同的电子层结构 | |
| C. | 39K和40Ca互为同位素 | |
| D. | 40K的原子半径小于40Ca 的原子半径 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
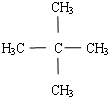 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 乙炔和苯 | B. | 甲烷和乙烷 | C. | 乙烯和丁炔 | D. | 苯和苯乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
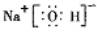 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
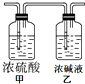 某有机物X相对氢气的密度为30,9g该有机物在空气中充分燃烧,燃烧产物依次通过右图所示的装置,实验结束后,称得甲装置增重5.4g,乙装置增重13.2g.通过计算,求
某有机物X相对氢气的密度为30,9g该有机物在空气中充分燃烧,燃烧产物依次通过右图所示的装置,实验结束后,称得甲装置增重5.4g,乙装置增重13.2g.通过计算,求查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com