
| ||
| A、只是被氧化 |
| B、只是被还原 |
| C、有的被氧化,有的被还原 |
| D、既未被氧化,也未被还原 |
科目:高中化学 来源: 题型:
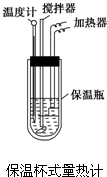 在量热计中(如图)将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.
在量热计中(如图)将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水的摩尔质量是18g |
| B、HCl的摩尔质量等于NA个HCl分子的质量 |
| C、摩尔是七个基本物理量之一 |
| D、1mol CO2的质量以克为单位时,在数值上等于CO2的相对分子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
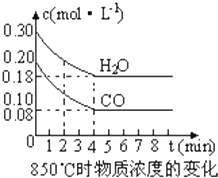 (1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将C(s)的表面积增大 |
| B、增大体系的压强 |
| C、升高体系的温度 |
| D、使用合适的催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使甲基橙呈红色的溶液:NH4+、Na+、Al02-、HC03- | ||
| B、c(NH3?H2O)=1.Omol?L-1的溶液:K+、Al3+、S042-、Cl- | ||
| C、由水电离的c(H+)=10-12mol?L-1的溶液:K+、Ba2+、Cl-、Br- | ||
D、在
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、极性键只能形成极性分子 |
| B、CO2中碳原子是sp2杂化 |
| C、形成配位键的条件是一方有空轨道,另一方有孤对电子 |
| D、共价键形成的条件是成键原子必须有未成对电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 新型纳米材料氧缺位铁酸盐(MFe2Ox 3<x<4,M=Mn、Co、Zn或Ni,在该盐中均显+2价)由铁酸盐(MFe2O4)经高温与氢气反应制得,常温下,它能使工业废气中的酸性氧化物(SO2、NO2等)转化为其单质除去,转化流程如图.关于此转化过程的叙述不正确的是( )
新型纳米材料氧缺位铁酸盐(MFe2Ox 3<x<4,M=Mn、Co、Zn或Ni,在该盐中均显+2价)由铁酸盐(MFe2O4)经高温与氢气反应制得,常温下,它能使工业废气中的酸性氧化物(SO2、NO2等)转化为其单质除去,转化流程如图.关于此转化过程的叙述不正确的是( )| A、MFe2O4在与H2的反应中表现了氧化性 |
| B、MFe2O4与MFe2Ox的相互转化反应均属于氧化还原反应 |
| C、MFe2Ox与SO2反应中MFe2Ox被还原 |
| D、若4 mol MFe2Ox与1 mol SO2恰好完全反应,则MFe2Ox中x的值为3.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com