
【题目】蒽的结构简式如右图(![]() )、联苯的结构简式如右图(
)、联苯的结构简式如右图(![]() ),下列 有关蒽和联苯的说法中正确的是( )
),下列 有关蒽和联苯的说法中正确的是( )
A. 联苯和蒽同属于芳香烃,两者互为同系物
B. 联苯的一氯代物有 3 种,蒽的二氯代物有 15 种
C. 1mol 蒽最多可以和 9molH2 发生加成反应
D. 联苯易发生加成反应、取代反应,也易溶于水
【答案】B
【解析】A项,联苯(![]() )和蒽(
)和蒽(![]() )均含苯环,只含C、H元素,都属于芳香烃,但环状结构不完全相同,二者不是同系物,故A错误;B项,联苯结构对称,分子中有3种H,则联苯的一氯代物有3种,蒽(
)均含苯环,只含C、H元素,都属于芳香烃,但环状结构不完全相同,二者不是同系物,故A错误;B项,联苯结构对称,分子中有3种H,则联苯的一氯代物有3种,蒽(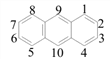 )的二氯代物:1、4、5、8称为α位;2、3、6、7称为β位;9、10位称为中位或者γ位。一个氯原子在α位,另一个可以在剩下的九个碳原子上,有9种(αCl-αCl、αCl-βCl、αCl-γCl三种类型);一个氯原子在β位,另一个可以在剩下的3个β位以及2个γ位碳原子上,有5种(βCl-βCl、γCl-βCl两种类型);一个氯原子在γ位,另一个可以在剩下的1个γ碳原子上,有1种,故B正确;C项,1mol 蒽最多可以和7molH2发生加成反应,故C错误;D项,联苯含苯环结构,易发生取代反应,难发生加成反应,烃类有机物大都难溶于水,故D错误。综上,选B。
)的二氯代物:1、4、5、8称为α位;2、3、6、7称为β位;9、10位称为中位或者γ位。一个氯原子在α位,另一个可以在剩下的九个碳原子上,有9种(αCl-αCl、αCl-βCl、αCl-γCl三种类型);一个氯原子在β位,另一个可以在剩下的3个β位以及2个γ位碳原子上,有5种(βCl-βCl、γCl-βCl两种类型);一个氯原子在γ位,另一个可以在剩下的1个γ碳原子上,有1种,故B正确;C项,1mol 蒽最多可以和7molH2发生加成反应,故C错误;D项,联苯含苯环结构,易发生取代反应,难发生加成反应,烃类有机物大都难溶于水,故D错误。综上,选B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】25℃时,用0.1000 mol/L KOH溶液滴定20.00 mL 0.1000 mol/L CH3COOH溶液,滴定中pH变化如图,下列关系错误的是

A.V=0.00mL时,CH3COOH溶液pH=3,其电离平衡常数K≈10-5mol/L
B.V=10.00mL时,溶液中2c(K+)=c(CH3COO-)+c(CH3COOH)
C.V≥20.00mL时,溶液中一定有c(K+)>c(CH3COO-)>c(OH-)> c(H+)
D.溶液pH=7时,![]() =1
=1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)制备铁红(Fe2O3)的生产流程如下:

试回答下列问题:
(1)步骤Ⅰ常需将烧渣粉碎、并加入过量H2SO4,其目的是 ;所得溶液中铁元素的化合价是 。
(2)步骤Ⅲ的目的是将溶液中的Fe3 +还原为Fe2 +,如何证明步骤Ⅲ已经进行完全 。步骤Ⅲ也可以加入FeS2代替铁粉的作用,请完成该反应的离子方程式:
FeS2 + 14Fe3 + + H2O=15Fe2 + + SO42- + 。
(3)步骤Ⅳ中可以选用试剂 调节溶液的pH(填字母编号)。
a.FeO固体 b.氢氧化钠溶液 c.Fe2O3固体 d.氨水
(4)步骤Ⅵ中发生反应的化学方程式为 。
(5)室温下FeCO3达到溶解平衡时溶液pH=8.5,c(Fe2+)=1.0×10-6 mol·L-1。通过计算说明FeCO3固体产物中是否含有Fe(OH)2 (已知:Ksp[Fe(OH)2]=4.8×10-16)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现,NOx和SO2是雾霾的主要成分。
Ⅰ.NOx主要来源于汽车尾气。
已知:N2(g) + 2O2(g)![]() 2NO2(g) ΔH=+67.5kJ/mol
2NO2(g) ΔH=+67.5kJ/mol
2CO(g) + O2(g)![]() 2CO2(g) ΔH=-566.00kJ/mol。
2CO2(g) ΔH=-566.00kJ/mol。
(1)为了减轻大气污染,在汽车尾气排气管口采用催化剂将NO2和CO转化成无污染气体参与大气循环。写出该反应的热化学方程式 。
(2)T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中发生反应2NO(g)+2CO(g)![]() 2CO2(g) +N2(g),保持温度和体积不变,反应过程(0~15min)中NO的物质的量随时间变化的关系如图所示。
2CO2(g) +N2(g),保持温度和体积不变,反应过程(0~15min)中NO的物质的量随时间变化的关系如图所示。


①下列能说明该反应达到平衡状态的是____________。
A.体系压强保持不变 B.NO和CO的转化率相等
C.混合气体的密度保持不变 D.混合气体的平均相对分子质量保持不变
②前10min以N2表示的化学反应速率v(N2)=_______________;T℃时该化学反应的平衡常数K=_______________;平衡时若保持温度不变,再向容器中充入CO、N2各0.8mol,平衡将_______移动(填“向左”、“向右”或“不)。15min时,若降低温度,导致n(NO)发生如图所示的变化,则该反应的ΔH 0(填“>”、“=”或“<”)。
Ⅱ.SO2主要来源于煤的燃烧。燃煤烟气的脱硫减排是减少大气中含硫化合物污染的关键。
(3)如图电解装置可将雾霾中的NO、SO2分别转化为NH4+和SO42-。
物质A的化学式为_____________,阴极的电极反应式是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学平衡常数说法中错误的是
A.某特定反应的平衡常数仅是温度的函数
B.化学平衡发生移动,平衡常数必发生改变
C.平衡常数发生变化,化学平衡必定发生移动
D.催化剂不能改变平衡常数的大小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com